
科目:高中化學 來源: 題型:解答題

| 離子 | Cu2+ | Fe2+ | Mg2+ |
| pH | 5.2 | 7.6 | 10.4 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ②④ | B. | ③ | C. | ①⑤②⑥ | D. | ③⑥ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | KClO3和KIO3均屬于離子化合物,含有離子鍵和共價鍵 | |
| B. | 為防止反應的尾氣造成大氣污染,可以用堿性溶液吸收尾氣 | |
| C. | 反應過程中I2置換出Cl2,由此可推斷非金屬性I>Cl | |
| D. | 制備KIO3的反應中I2被氧化 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
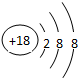 .元素⑩名稱為溴單質與水反應化學方程式Br2+H2O=HBr+HBrO.
.元素⑩名稱為溴單質與水反應化學方程式Br2+H2O=HBr+HBrO.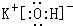 .
.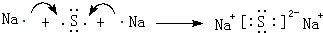 ,該化合物屬于離子(填“共價”或“離子”)化合物.
,該化合物屬于離子(填“共價”或“離子”)化合物.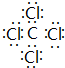 、
、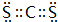 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用A表示的反應速率是0.4 mol/(L•min) | |
| B. | 分別用B、C表示反應的速率,其比值是3:2 | |
| C. | 在2 min末的反應速率,用B表示是0.3 mol/(L•min) | |
| D. | 在這2 min內B和C兩物質濃度都逐漸減小 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2H2(g)+O2(g)═2H2O(l);△H1 2H2(g)+O2(g)═2H2O(g);△H2 | |
| B. | 2S(g)+O2(g)═2SO2(g);△H1 2S(s)+O2(g)═2SO2(g);△H2 | |
| C. | C(s)+$\frac{1}{2}$O2(g)═CO(g);△H1C(s)+O2(g)═CO2(g);△H2 | |
| D. | H2(g)+Cl2(g)═2HCl(g);△H1 $\frac{1}{2}$H2(g)+$\frac{1}{2}$Cl2(g)═HCl(g);△H2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com