
【題目】下列各組離子可能大量共存的是
A.常溫下Kw/c(H+)=1×10-13mol·L-1的溶液中:Ca2+、Fe2+、NO![]() 、NH
、NH![]()
B.水電離出的c(H+)=10-10mol·L—1的溶液中Na+、K+、Cl、HCO3
C.pH=11的溶液中:CO32-、Na+、AlO2-、NO3-、S2-、SO32-
D.c(Fe3+)=0.1mol·L-1的溶液中:K+、Cl-、SO42-、H2O2
科目:高中化學 來源: 題型:
【題目】燃料電池是符合綠色化學理念的新型發電裝置。下圖為氫氧燃料電池示意圖,該電池電極表面鍍一層細小的鉑粉,鉑吸附氣體的能力強,性質穩定,請回答:
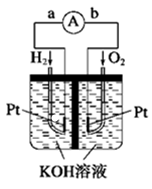
(1)氫氧燃料電池的能量轉化主要形式是 ,在導線中電子流動方向為 (用a、b 表示)。
(2)負極反應式為 ,正極反應式為 ;
(3)該電池工作時,H2和O2連續由外部供給,電池可連續不斷提供電能。因此,大量安全儲氫是關鍵技術之一。金屬鋰是一種重要的儲氫材料,吸氫和放氫原理如下:
Ⅰ.2Li+H2![]()
![]() 2LiH Ⅱ.LiH+H2O
2LiH Ⅱ.LiH+H2O![]() LiOH+H2↑
LiOH+H2↑
反應Ⅰ中的還原劑是 ,反應Ⅱ中的氧化劑是 ;
(4)如果該電池是甲烷-氧氣燃料電池,負極反應式為 ;
(5)如果該電池是肼(N2H4)-氧氣燃料電池,負極反應式為 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在不同條件下分別測得反應2SO2(g)+O2(g) ![]() 2SO3(g)的化學反應速率,其中表示該反應進行的最快的是
2SO3(g)的化學反應速率,其中表示該反應進行的最快的是
A.v(SO2)=4 mol·L-1·min-1 B.v(O2)=3 mol·L-1·min-1
C.v(SO2)=0.1 mol·L-1·s-1 D.v(O2)=0.1 mol·L-1·s-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】ClO2氣體是一種常用的消毒劑,我國從2 000年起逐步用ClO2代替氯氣對飲用水進行消毒。
(1)消毒水時,ClO2還可將水中的Fe2+、Mn2+等轉化成Fe(OH)3和MnO2等難溶物除去,在這個過程中,Fe2+、Mn2+的化合價升高,說明ClO2具有__________性。
(2)工業上可以通過下列方法制取ClO2,請完成該化學反應方程式:
2KClO3+SO2=2ClO2+__________。
(3)使Cl2和H2O(g)通過灼熱的炭層,生成HCl和CO2,是放熱反應,當1 mol Cl2參與反應時 釋放145 kJ的熱量,寫出這個反應的熱化學方程式:________________。
(4)自來水廠用ClO2處理后的水中,要求ClO2的濃度在0.1~0.8 mg·L-1之間。碘量法可以檢 測水中ClO2的濃度,步驟如下:
Ⅰ.取一定體積的水樣,加入一定量的碘化鉀,再用氫氧化鈉溶液調至中性,并加入淀粉溶液,溶液變藍。
Ⅱ.加入一定量的Na2S2O3溶液。(已知:2S2O![]() +I2=S4O
+I2=S4O![]() +2I-)
+2I-)
Ⅲ.加硫酸調節水樣pH至1~3。
操作時,不同pH環境中粒子種類如下圖所示:

請回答:
①操作Ⅰ中反應的離子方程式是___________________。
②確定操作Ⅱ完全反應的現象是___________________。
③在操作Ⅲ過程中,溶液又呈藍色,反應的離子方程式是___________________。
④若水樣的體積為1.0L,在操作Ⅱ時消耗了1.0×10-3mol·L-1的Na2S2O3溶液10mL,則水樣中ClO2的濃度是________mg·L-1。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在標準狀況下,將a L NH3完全溶于水得到V mL氨水,溶液的密度為ρ g·cm-3,溶質的質量分數為w,溶質的物質的量濃度為c mol·L-1。下列敘述中正確的是
①若上述溶液中再加入等體積水后,所得溶液的質量分數大于0.5w
②c=![]()
③w=![]() ×100%
×100%
④若上述溶液中再加入0.5V mL同濃度稀鹽酸,充分反應后,溶液中離子濃度大小關系為c(NH4+)>c(Cl-)>c(OH-)>c(H+)
A. ①④ B. ②③ C. ①③ D. ②④
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知反應FeO(s)+CO(g) ![]() Fe(s)+CO2(g) 的Kc=0.5(1273K)。若起始濃度c(CO)=0.05 mol·L-1,c(CO2)=0.01 mol·L-1,請回答:
Fe(s)+CO2(g) 的Kc=0.5(1273K)。若起始濃度c(CO)=0.05 mol·L-1,c(CO2)=0.01 mol·L-1,請回答:
(1)判斷化學反應進行的方向并計算反應物、生成物的平衡濃度。
(2)CO的轉化率是多少?
(3)增加FeO的量,對平衡有無影響?
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】X、Y、Z、R、Q、M是六種短周期元素,原子序數依次增大。X是原子半徑最小的元素,Y的氣態氫化物能使濕潤的紅色石蕊試紙變藍,Z為地殼中含量最多的元素,R與X同主族;Y、R、Q最外層電子數之和為8,M的單質黃綠色有害氣體。請回答下列問題:
(1)R在元素周期表中的位置為___________。
(2)Z、Q、M簡單離子半徑由大到小的順序為(寫元素離子符號)_________________。
(3)YX4M的電子式為___________,Q3Y2與水可劇烈反應,反應的化學方程式為____________
(4)M的單質與R的最高價氧化物對應的水化物反應的離子方程式為___________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】二甘醇可用作溶劑、紡織助劑等,一旦進入人體會導致急性腎衰竭,危及生命。二甘醇的結構簡式是HOCH2CH2OCH2CH2OH。下列有關二甘醇的敘述正確的是
A.符合通式CnH2nO3
B.能溶于水,不溶于乙醇
C.分子間不存在范德華力
D.分子間能形成氫鍵
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com