
| A. | 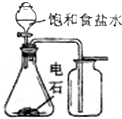 實驗室制備并收集乙炔 | B. | 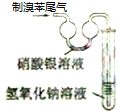 證明溴苯中含溴元素 | ||
| C. | 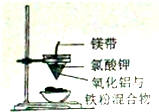 鋁熱反應 | D. | 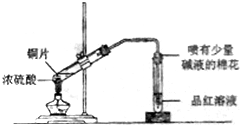 檢測銅與濃硫酸反應的氣體產物 |
分析 A.電石與水反應生成乙炔,乙炔的密度與空氣的密度接近,不能利用排空氣法收集;
B.溴苯與硝酸銀不反應;
C.鋁熱反應為Al與金屬氧化物反應;
D.Cu與濃硫酸發(fā)生氧化還原反應生成二氧化硫,二氧化硫具有漂白性,且污染環(huán)境.
解答 解:A.電石與水反應生成乙炔,乙炔的密度與空氣的密度接近,不能利用排空氣法收集,應利用排水法收集,圖中收集方法不合理,故A錯誤;
B.溴苯與硝酸銀不反應,不能檢驗溴苯中含溴元素,故B錯誤;
C.鋁熱反應為Al與金屬氧化物反應,圖中為鐵與氧化鋁,二者不反應,故C錯誤;
D.Cu與濃硫酸發(fā)生氧化還原反應生成二氧化硫,二氧化硫具有漂白性,且污染環(huán)境,則品紅褪色,含堿液的棉花可吸收尾氣,故D正確;
故選D.
點評 本題考查化學實驗方案的評價,為高頻考點,涉及氣體的制備及收集、有機物的結構與性質、鋁熱反應等,把握物質的性質、反應原理、實驗裝置的作用等為解答的關鍵,側重分析與實驗能力的考查,注意實驗的評價性分析,題目難度不大.


科目:高中化學 來源: 題型:選擇題
| A. | Ne、H2、O2 | B. | O2、N2、H2 | C. | NO、CO2、H2 | D. | NH3、O2、NO2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. |  | B. |  | C. |  | D. |  |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 實驗室可用丁達爾效應鑒別膠體與溶液 | |
| B. | “雨后彩虹”既是一種自然現(xiàn)象又是光學現(xiàn)象,同時也與膠體有關 | |
| C. | 在溶有1mol Fe(OH)3的膠體中,含有NA個Fe(OH)3膠粒 | |
| D. | 分散質粒子大小介于1~100nm之間的分散系稱為膠體 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 實驗室制備1,2-二溴乙烷的反應原理如下:
實驗室制備1,2-二溴乙烷的反應原理如下:| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 狀態(tài) | 無色液體 | 無色液體 | 無色液體 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸點/℃ | 78.5 | 132 | 34.6 |
| 熔點/℃ | 一l30 | 9 | -1l6 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 32g SO2所含的原子數(shù)目為1.5NA | |
| B. | 0.5molCH4含有的原子數(shù)目為2.5N:x | |
| C. | 10g H2O含有的水分子數(shù)目為NA | |
| D. | 0.5NA個氯氣分子的物質的量是0.5mol |
查看答案和解析>>
湖北省互聯(lián)網違法和不良信息舉報平臺 | 網上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com