
| A. | PH大小順序①>④>③>② | |
| B. | C(NH3•H2O)大小順序:②>④>③>① | |
| C. | 混合溶液④中存在C(NH3•H2O)+C(CO32-)+C(H+)=C(OH-)+C(H2CO3) | |
| D. | 混合溶液③中水的電離被促進,其中C(H+)和C(OH-)均大于1.0×10-7mol/L |
分析 A、根據銨根離子的水解程度來確定溶液酸堿性的強弱.
B、①NH4Cl與NaOH反應生成氯化鈉和一水合氨,②NH4Cl中銨根離子水解生成一水合氨,鹽酸抑制其水解,③氯化鈉對銨根離子的水解無影響,④碳酸氫鈉對銨根離子水解起到促進作用;
C、混合溶液中的守恒思想來回答;
D、③中NH4Cl的水解促進水的電離.
解答 解:A、①NH4Cl與NaOH反應生成氯化鈉和一水合氨,一水合氨電離導致溶液顯示堿性,堿性最強,②NH4Cl與 HCl混合液顯示酸性,③氯化鈉對銨根離子的水解無影響,銨根水解顯示酸性,④醋酸銨溶液的PH=7,所以醋酸根離子和銨根離子水解程度相同,碳酸氫根水解程度大于銨根的水解程度,溶液顯示堿性,即C(OH-)>C(H+),所以PH大小順序為:①>④>③>②,故A正確;
B、①NH4Cl與NaOH反應生成等濃度的氯化鈉和一水合氨,②NH4Cl中銨根離子水解生成一水合氨,鹽酸抑制其水解,③NH4Cl中銨根離子水解生成一水合氨,氯化鈉對銨根離子的水解無影響,④NH4Cl中銨根離子水解生成一水合氨,碳酸氫鈉對銨根離子水解起到促進作用,所以一水合氨的濃度大小順序是:①>④>②>③,故B錯誤;
C、NH4Cl與 NaHCO3 的混合溶液中,C(HCO3-)+2C(CO32-)+C(OH-)+C(Cl-)=C(H+)+C(Na+)+C(NH4+),C(NH4+)+C(NH3•H2O)=C(Cl-),C(HCO3-)+C(CO32-)+C(H2CO3)=C(Na+),且C(Cl-)=C(Na+),聯立以上等式可得:C(NH3•H2O)+C(CO32-)+C(OH-)=C(H+)+C(H2CO3),故C錯誤;
D、③中NH4Cl水解結合了水電離出的OH-,對水的電離有促進作用,故溶液中的氫離子的濃度大于10-7mol/L,但由于OH-被結合,故溶液中氫氧根的濃度小于10-7mol/L,故D錯誤.
故選A.
點評 本題是一道關于離子濃度大小比較以及離子濃度之間關系知識的綜合題,涉及鹽的水解規律、弱電解質的電離平衡等方面的知識,綜合性較強,難度大.


 沖刺100分1號卷系列答案
沖刺100分1號卷系列答案 期末好成績系列答案
期末好成績系列答案科目:高中化學 來源: 題型:解答題
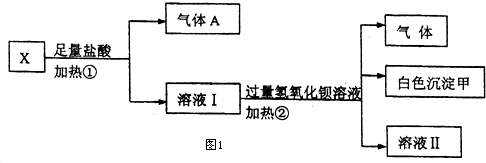
| 陽離子 | Na+、K+、Cu2+ |
| 陰離子 | SO${\;}_{4}^{2-}$、OH- |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 10L | B. | 15L | C. | 25L | D. | 27L |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
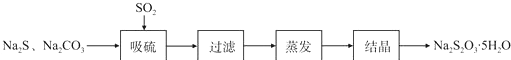
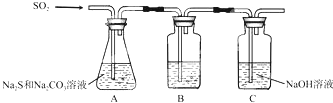
| 序號 | 實驗操作 | 預期現象 | 結論 |
| ① | 取少量樣品于試管中,加入適量蒸餾水,充分振蕩溶解 滴加足量稀硝酸,再滴加少量AgNO3溶液,振蕩 | 有白色沉淀生成 | 樣品含NaCl |
| ② | 取少量樣品于試管中,加入適量蒸餾水,充分振蕩溶解 加入過量BaCl2溶液,攪拌,靜置,用pH計測定上層清液pH | 有白色沉淀生成,上層清液pH大于9.6 | 樣品含NaOH |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 敘述 | 評價 |
| A | 乙酸乙酯在H218 O中水解,產物乙醇中將含有18O | 錯,根據酯的水解規律,產物乙酸中將含有18O同位素,而乙醇則沒有. |
| B | 淀粉與20%的硫酸混合溶液在沸水浴中充分加熱后滴加碘水無藍色現象,則說明淀粉水解完全 | 錯,淀粉水解后未加堿中和至溶液呈堿性. |
| C | 向鹵代烴水解后的溶液中加入AgNO3溶液,根據沉淀顏色可以判斷鹵素原子種類 | 對,水解后溶液中有鹵化氫,與AgNO3溶液反應生成鹵化銀沉淀. |
| D | 可以用新制的Cu(OH)2懸濁液鑒別乙醇溶液、乙酸溶液和葡萄糖溶液 | 錯,用新制的Cu(OH)2懸濁液不能鑒別乙醇溶液和乙酸溶液. |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com