
| 溶質 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
| PH | 8.1 | 8.4 | 11.6 | 10.3 | 11.1 | 11.3 |


 學期復習一本通學習總動員期末加暑假延邊人民出版社系列答案
學期復習一本通學習總動員期末加暑假延邊人民出版社系列答案 芒果教輔暑假天地重慶出版社系列答案
芒果教輔暑假天地重慶出版社系列答案科目:高中化學 來源: 題型:
| A、N2O4和NO2的分子數比為1:2 |
| B、N2O4和NO2的濃度相等 |
| C、平衡體系的顏色一定不再改變 |
| D、單位時間有1 mol N2O4變為NO2的同時,有2 mol NO2變為N2O4 |
查看答案和解析>>
科目:高中化學 來源: 題型:

| 沉淀物 | Al(OH)3 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
| pH | 5.2 | 3.2 | 9.7 | 6.7 |
| H2 |
| 550℃ |
查看答案和解析>>
科目:高中化學 來源: 題型:
| 物質 性質 | 與NaOH溶液 | 與銀氨溶液 | 與鈉 |
| A | 水解 | 不產生銀鏡 | 不反應 |
| B | 中和 | 不產生銀鏡 | 產生H2 |
| C | 水解 | 產生銀鏡 | 不反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| ||

查看答案和解析>>
科目:高中化學 來源: 題型:

查看答案和解析>>
科目:高中化學 來源: 題型:
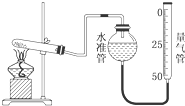 某學生利用高錳酸鉀分解制氧氣的反應,測定室溫下的氣體摩爾體積,實驗裝置如圖所示.部分實驗步驟:①裝好實驗裝置.②…③把適量的高錳酸鉀粉末放入干燥的試管中,準確稱量試管和高錳酸鉀粉末的質量為a g.④加熱,開始反應,直到產生一定量的氣體.⑤停止加熱.⑥測量收集到的氣體的體積.⑦準確稱量試管和殘留物的質量為b g.⑧測量實驗室的溫度.回答下列問題.
某學生利用高錳酸鉀分解制氧氣的反應,測定室溫下的氣體摩爾體積,實驗裝置如圖所示.部分實驗步驟:①裝好實驗裝置.②…③把適量的高錳酸鉀粉末放入干燥的試管中,準確稱量試管和高錳酸鉀粉末的質量為a g.④加熱,開始反應,直到產生一定量的氣體.⑤停止加熱.⑥測量收集到的氣體的體積.⑦準確稱量試管和殘留物的質量為b g.⑧測量實驗室的溫度.回答下列問題.查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com