
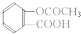

分析 (1)①鋼是鐵與碳的合金;鐵銹蝕主要發生的是電化學腐蝕,其負極發生氧化反應鐵失去電子生成二價鐵離子;無機非金屬材料是以某些元素的氧化物、碳化物、氮化物、鹵素化合物、硼化物以及硅酸鹽、鋁酸鹽、磷酸鹽、硼酸鹽等物質組成的材料.常見的有玻璃、水泥、陶瓷等;
②依據真絲織品成分為蛋白質,化纖織品是不添加純天然纖維材料,純粹由滌綸、錦綸、氨綸、丙綸、維綸、腈綸、粘膠、尼龍、醋酸纖維、天絲等材料中的一種或幾種合成的布料制成的衣物,依據其性質判斷解答;
(2)①含鉀、鈉、鈣、鎂等礦物質較多的食物,在體內的最終的代謝產物常呈堿性,產生堿性物質的稱為堿性食品,蔬菜、水果、乳類、大豆和菌類食物等;加碘鹽中添加的為碘酸鉀;二價鐵離子若變質則被氧化生成三價鐵離子,三價鐵離子遇到硫氰酸鉀顯血紅色;
②氫氧化鋁能夠與鹽酸反應消耗氫離子;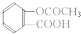 含有羧基和酯基;
含有羧基和酯基;
(3)①CO與NO在催化劑作用下生成氮氣和二氧化碳;
②漂白粉與空氣接觸后,會和二氧化碳水反應生成碳酸鈣和次氯酸,次氯酸具有強氧化性,能進行殺菌消毒漂白;
③選用能夠降解的塑料袋,為了防止不能降解而帶來的環境污染;把垃圾分為可回收物和不可回收物.
解答 解:(1)①鋼是鐵與碳的合金;
鐵銹蝕主要發生的是電化學腐蝕,其負極發生氧化反應鐵失去電子生成二價鐵離子,電極反應式為:Fe-2e-=Fe2+;
常見的有玻璃、水泥、陶瓷等;
故答案為:鐵合金;Fe-2e-=Fe2+;陶瓷;
②A.真絲織品主要成分為蛋白質,主要含有C,H,O,N四種元素,故A正確;
B.真絲制品含有蛋白質灼燒產生燒焦羽毛的氣味,化纖織品不具有此性質,故B正確;
C.真絲織品中成分遇到重金屬鹽,強酸,強堿,有機物等會產生沉淀而失去活性,化纖織品不含蛋白質不具有此性質,故C錯誤;
D.兩種產品都屬于高分子材料,故D正確;
故選:C;
(2)①水果為堿性食物;加碘鹽是指在食鹽中加適量的碘酸鉀;二價鐵離子若變質則被氧化生成三價鐵離子,三價鐵離子遇到硫氰酸鉀顯血紅色,所以檢驗亞鐵丸是否變質方法:刮去藥片上的糖衣,把藥片碾碎,放入燒杯中,溶解,過濾后向濾液中加入硫氰酸鉀,如果溶液變紅色,說明已經變質,如果溶液沒變紅色說明沒變質;
故答案為:水果;碘酸鉀;刮去藥片上的糖衣,把藥片碾碎,放入燒杯中,溶解,過濾后向濾液中加入硫氰酸鉀,如果溶液變紅色,說明已經變質,如果溶液沒變紅色說明沒變質;
②氫氧化鋁能夠與鹽酸反應消耗氫離子,所以可以用來治療胃酸過多;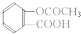 含有羧基和酯基;
含有羧基和酯基;
故答案為:胃酸過多;羧基;
(3)①CO與NO在催化劑作用下生成氮氣和二氧化碳,方程式:2CO+2NO$\frac{\underline{\;催化劑\;}}{\;}$2CO2+N2;
故答案為:2CO+2NO$\frac{\underline{\;催化劑\;}}{\;}$2CO2+N2;
②碳酸酸性強于次氯酸,漂白粉與空氣接觸后,會和二氧化碳水反應生成碳酸鈣和次氯酸,次氯酸具有強氧化性,能進行殺菌消毒漂白,反應的化學方程式為:Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO,
故答案為:Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO;
③塑料不易降解,影響環境的美觀,所含成分有潛在危害,塑料用做包裝材料多為白色,往往稱為白色污染;可回收物可以重復利用,所以循環圖標,
故答案為:白色污染;可回收物.
點評 本題為綜合題,考查課生活中常見的化學知識,設計環境污染與治理、生活中常見的材料類型及性質、食品與藥物等,題目難度不大,注意對相關知識的積累.


科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①②③④⑤ | B. | ②③④⑤⑥ | C. | ②③⑤⑥⑦ | D. | ①②⑤⑥⑦ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | a=1,b=2 | B. | a=2,b=1 | C. | a=2,b=2 | D. | a=3,b=2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 10g H2和10g O2 | B. | 標準狀況下相同體積的N2和H2 | ||
| C. | 9g水和0.25mol H2 | D. | 22g CO2和3.01×1023個N2 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com