
【題目】(1)元素的第一電離能:Al____Si(填“>”或“<”),按電負性由大到小的順序排列N、O、F___。
(2)基態Mn2+的核外電子排布式為___。
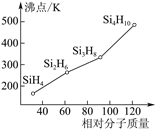
(3)硅烷(SinH2n+2)的沸點與其相對分子質量的變化關系如圖所示,呈現這種變化關系的原因是___。
(4)硼砂是含結晶水的四硼酸鈉,其陰離子Xm-(含B、O、H三種元素)的球棍模型如圖所示:
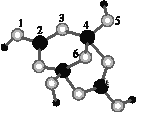
①在Xm-中,硼原子軌道的雜化類型有___;配位鍵存在于___原子之間(填原子的數字標號)。
②硼砂晶體由Na+、Xm-和H2O構成,它們之間存在的作用力有___(填序號)。
A.離子鍵 B.共價鍵 C.金屬鍵 D.范德華力E.氫鍵
【答案】< F>O>N 1s22s22p63s23p63d5(或[Ar]3d5) 硅烷的相對分子質量越大,分子間范德華力越強 sp2、sp3 4,5(或5,4) ABDE
【解析】
(1)同周期從左到右第一電離能逐漸增大趨勢,第ⅡA和第ⅤA族則反常;同周期元素,從左到右電負性增強;
(2)Mn的電子排布式為1s22s22p63s23p63d54s2或[Ar]3d54s2;
(3)硅烷是分子晶體,結構相似,相對分子質量越大,分子間的范德華力越大,沸點越高;
(4)①1,3,5,6代表氧原子,2,4代表B原子,2號B形成3個鍵,則B原子為sp2雜化,4號B形成4個鍵,則B原子為sp3雜化; B一般是形成3個鍵,4號B形成4個鍵,其中1個鍵很可能就是配位鍵,配位鍵存在4號與5號之間;
②鈉離子與Xm-形成離子鍵,水分子由共價鍵形成,結晶水分子間存在氫鍵和范德華力。
(1)同周期從左到右第一電離能逐漸增大趨勢,第ⅡA和第ⅤA族則反常,所以鋁的第一電離能小于硅的;同周期元素,從左到右電負性增強,N、O、F電負性由大到小的順序是F>O>N ,故答案為:<;F>O>N ;
(2)Mn的電子排布式為1s22s22p63s23p63d54s2或[Ar]3d54s2,則基態Mn2+的核外電子排布式為1s22s22p63s23p63d5或[Ar]3d5,故答案為:1s22s22p63s23p63d5(或[Ar]3d5);
(3)硅烷是分子晶體,結構相似,相對分子質量越大,分子間的范德華力越大,沸點越高,故答案為:硅烷的相對分子質量越大,分子間范德華力越強;
(4)①1,3,5,6代表氧原子,2,4代表B原子,2號B形成3個鍵,則B原子為sp2雜化,4號B形成4個鍵,則B原子為sp3雜化; B一般是形成3個鍵,4號B形成4個鍵,其中1個鍵很可能就是配位鍵,配位鍵存在4號與5號之間,故答案為:sp2、sp3;4,5(或5,4);
②鈉離子與Xm-形成離子鍵,水分子由共價鍵形成,結晶水分子間存在氫鍵和范德華力,故答案為:ABDE。


科目:高中化學 來源: 題型:
【題目】設NA為阿伏加德羅常數,下列有關說法正確的是( )
A.0.5mol羥基中所含電子數為5NA
B.標況下,11.2LCHCl3中,共用電子對的數目為2NA
C.2.8g的乙烯和丙烯(C3H6)中含有的碳原子數為0.2NA
D.1mol苯乙烯(![]() )分子中含有碳碳雙鍵的個數為4NA
)分子中含有碳碳雙鍵的個數為4NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氮、硫的化合物合成、應用以及對環境的影響一直是科學界研究的熱點。
(1)尿素主要以NH3和CO2為原料進行合成。主要通過以下兩個反應進行:
反應1:2NH3(l)+CO2(g)![]() H2NCOONH4(l) ΔH1= -117.2 kJ·mol-1
H2NCOONH4(l) ΔH1= -117.2 kJ·mol-1
反應2:H2NCOONH4(l)![]() H2O(l)+CO(NH2)2(l) ΔH2=+21.7 kJ·mol-1
H2O(l)+CO(NH2)2(l) ΔH2=+21.7 kJ·mol-1
請回答:CO(NH2)2 (l)+H2O(l)![]() 2NH3(l)+CO2(g) ΔH3=_____________,該反應能自發進行的主要原因是__________________.
2NH3(l)+CO2(g) ΔH3=_____________,該反應能自發進行的主要原因是__________________.
(2)焦炭催化還原SO2生成S2,化學方程式為:2C(s)+2SO2(g)![]() S2(g)+2CO2(g),在恒容容器中,1 mol/LSO2與足量的焦炭反應,SO2的轉化率隨溫度的變化如圖所示。
S2(g)+2CO2(g),在恒容容器中,1 mol/LSO2與足量的焦炭反應,SO2的轉化率隨溫度的變化如圖所示。
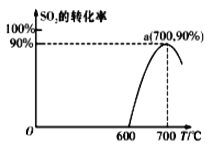
①若700℃發生該反應,經3分鐘達到平衡,計算0—3分鐘v(S2)=_______molL-1min-1,該溫度下的平衡常數為_________.
②若該反應在起始溫度為700℃的恒容絕熱容器中進行,達到平衡時SO2的轉化率________90%(填“>”、“<”或“=”).
③下列說法一定能說明該反應達到平衡狀態的是_______.
A.焦炭的質量不再變化時
B.CO2、SO2的濃度相等時
C.SO2的消耗速率與CO2的生成速率之比為1:1
D.容器的總壓強不再變化時
(3) NO2、O2和熔融KNO3可制作燃料電池,其原理如圖所示.

石墨I附近發生的反應為__________________________________,當外電路通過1mole-,正極上共消耗_______mol N2O5 。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在含有弱電解質的溶液中,往往有多個化學平衡共存。
(1)一定溫度下,向1L0.1molL﹣1CH3COOH溶液中加入0.1molCH3COONa固體,平衡后則溶液中![]() ___(填“增大”、“減小”或“不變”);寫出表示該混合溶液中所有離子濃度間的一個等式:______
___(填“增大”、“減小”或“不變”);寫出表示該混合溶液中所有離子濃度間的一個等式:______
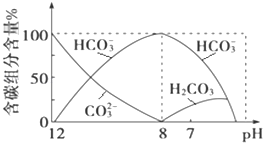
(2)常溫下向20mL 0.1molL﹣1Na2CO3溶液中逐滴加入0.1molL﹣1HCl溶液40mL,溶液中含碳元素的各種微粒(CO2因逸出未畫出)物質的量分數隨溶液pH變化的情況如下:
回答下列問題:
①在同一溶液中,H2CO3、HCO3﹣、CO32﹣___(填“能”或“不能”)大量共存;
②當pH=7時,溶液中含碳元素的主要微粒有_____、___,溶液中含量最多的三種微粒的物質的量濃度的大小關系為____;
③已知在25℃時,CO32﹣水解反應的平衡常數即水解常數Kh═2×10﹣4 molL﹣1,當溶液中c(HCO3﹣):c(CO32﹣)=2:1時,溶液的pH=_____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】NiCl2是化工合成中最重要的鎳源。工業上利用含鎳(Ni)廢催化劑(主要含有Ni,還含有SiO2、Al2O3、Fe及其它不溶于酸、堿的雜質)生產氯化鎳晶體(NiCl2·nH2O)流程如圖:
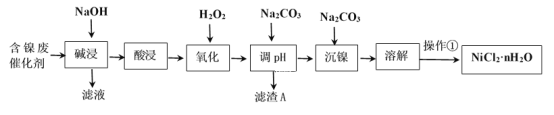
部分金屬氫氧化物Ksp近似值如下表所示:
化學式 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Ni(OH)2 |
Ksp近似值 | 10-17 | 10-38 | 10-34 | 10-15 |
回答下列問題:
(1)Al的原子結構示意圖為___。
(2)“酸浸”、“溶解”所使用的酸為___。“堿浸”時發生反應的離子方程式為SiO2+2OH-=SiO32-+H2O、____。
(3)“氧化”加入H2O2溶液,其作用是___(用離子方程式表示)。然后調節pH使溶液中鐵元素恰好完全沉淀(離子濃度≤10-5mol·L-1時,離子沉淀完全),此時常溫下的pH約為____。
(4)“操作①”的實驗操作依次為緩緩加熱,濃縮至___為止、冷卻結晶、過濾、洗滌、干燥,即得產品。
(5)鎳氫電池已成為混合動力汽車的主要電池類型,其在堿性電解質溶液的工作原理如下:M+Ni(OH)2![]() MH+NiOOH(式中M為儲氫合金)。寫出電池充電過程中陽極的電極反應式___。
MH+NiOOH(式中M為儲氫合金)。寫出電池充電過程中陽極的電極反應式___。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】若NA表示阿伏加德羅常數,下列說法中正確的是
A.在28g乙烯分子中,一定共平面的原子數目為6NA
B.1mol甲烷或白磷(P4)分子中所含的共價鍵數均為4NA
C.25℃時,1LpH=1的H2SO4溶液中含有的H+數為0.2NA
D.標準狀況下,22.4L氯氣與足量氫氧化鈉溶液反應,轉移的電子數為2NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】美托洛爾是一種治療高血壓的藥物的中間體,可以通過以下方法合成:
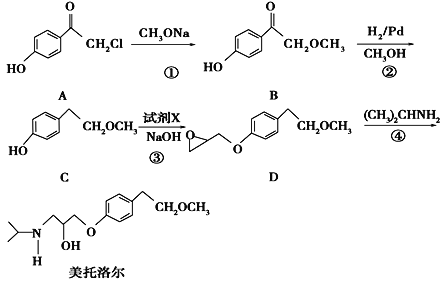
請回答下列問題:
(1)寫出C中的官能團的名稱為_________________.
(2)美托洛爾的分子式________________.
(3)寫出反應①的化學方程式__________________________________________;反應②的反應類型是_____________
(4)反應③中加入的試劑X的分子式為C3H5OCl,X的結構簡式為____________________.
(5)滿足下列條件的B的同分異構體有有_______種,其中核磁共振氫譜有六種不同化學環境的氫,且峰面積比為3∶2∶2∶1∶1∶1的是________________________(寫結構簡式)
①能發生銀鏡反應而且能發生水解
②能與FeCl3溶液發生顯色反應
③只有一個甲基
(6)根據已有知識并結合題目所給相關信息,寫出以![]() 和
和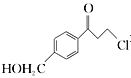 為原料制備
為原料制備![]() 的合成路線流程圖(無機試劑任選)。合成路線流程圖示例如下:
的合成路線流程圖(無機試劑任選)。合成路線流程圖示例如下:![]() _______________________
_______________________
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】秋冬季是霧霾高發的季節,其中汽車尾氣和燃煤尾氣是造成霧霾的主要原因之一。
(1)工業上利用甲烷催化還原NO,可減少氮氧化物的排放。
已知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)ΔH=-574kJ·mol1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)ΔH=-1160kJ·mol1
甲烷直接將NO2還原為N2的熱化學方程式為_____________________________________。
(2)汽車尾氣催化凈化是控制汽車尾氣排放、減少汽車尾氣污染的最有效的手段,主要原理為2NO(g)+2CO(g)![]() N2(g)+2CO2(g)ΔH<0
N2(g)+2CO2(g)ΔH<0
T℃時,將等物質的量的NO和CO充入容積為2L的密閉容器中,保持溫度和體積不變,反應過程(0~15min)中NO的物質的量隨時間變化如上圖所示。
①已知:平衡時氣體的分壓=氣體的體積分數×體系的總壓強,T℃時達到平衡,此時體系的總壓強為p=20MPa,則T℃時該反應的壓力平衡常數Kp=_______;平衡后,若保持溫度不變,再向容器中充入NO和CO2各0.3mol,平衡將_____(填“向左”、“向右”或“不”)移動。
②15min時,若改變外界反應條件,導致n(NO)發生如圖所示的變化,則改變的條件可能是__(填序號)
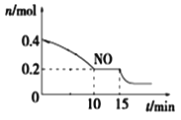
A.增大CO濃度B.升溫C.減小容器體積D.加入催化劑
(3)工業上常采用“堿溶液吸收”的方法來同時吸收SO2,和氮的氧化物氣體(NOx),如用氫氧化鈉溶液吸收可得到Na2SO3、NaHSO3、NaNO2、NaNO3等溶液。已知:常溫下,HNO2的電離常數為Ka=7×10-4,H2SO3的電離常數為Ka1=1.2×10-2、Ka2=5.8×10-8。
①常溫下,相同濃度的Na2SO3、NaNO2溶液中pH較大的是______溶液。
②常溫下,NaHSO3顯___性(填“酸”“堿”或“中”,判斷的理由是(通過計算說明)_____________。
(4)鈰元素(Ce)是鑭系金屬中自然豐度最高的一種,常見有+3、+4兩種價態。霧霾中含有大量的污染物NO,可以被含Ce4+的溶液吸收,生成NO2-、NO3-(二者物質的量之比為1∶1)。可采用電解法將上述吸收液中的NO2-轉化為無毒物質,同時再生Ce4+,其原理如圖所示。
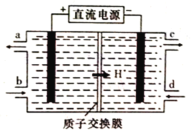
①Ce4+從電解槽的_____(填字母代號)口流出。
②寫出陰極的電極反應式:_______________________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定量的甲烷燃燒產物為CO、CO2和水蒸氣,此混合氣體重49.6g,當其緩慢通過無水CaCl2時,CaCl2增重25.2g,則原混合氣體中CO的質量為( )
A.11.2gB.13.2gC.19.7gD.24.4g
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com