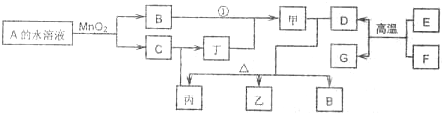
已知①~④均為工業生產及應用的常見反應.其中常溫下B、D、J、P氣體,E為分子中原子個數比為1:l的液體.A的相對分子質量為120.(個別反應的產物已略去)

試回答下列問題:
(1)反應F與N溶液反應的離子方程式為
2Al+2OH-+2H20=2AlO2-+3H2↑
2Al+2OH-+2H20=2AlO2-+3H2↑
;
(2)反應⑤中當有1mol電子轉移時,氧化劑消耗
17g
17g
g;
(3)反應④的離子方程式為
;如圖2是該反應原理的示意圖,該裝置中使用的是
陽
陽
(填“陰”或“陽”)離子交換膜,圖中從d處收集到的是
NaOH溶液
NaOH溶液
.
(4)工業上由D制取I的過程可表示為:

由D與B反應生成X的反應所用的設備是
③
③
;
①高爐 ②沸騰爐 ③接觸室 ④分餾塔 ⑤吸收塔
已知400℃101Kpa時,2D(g)+B(g?2X(g);△H=-196.6KJ/mol,當2mol D與1mol B在該條件下反應達平衡時反應放熱186.8KJ.在實際生產中綜合考慮各種因素,為提高D的轉化率,工業選擇了以下哪些條件
④⑤⑥
④⑤⑥
.
①適當升高溫度 ②增大壓強 ③使用合適的催化劑 ④及時移走生成物
⑤適當增大B的濃度 ⑥將反應物與生成物在熱交換器中進行熱交換.





 習題精選系列答案
習題精選系列答案