
分析 在C2H2(氣態)完全燃燒生成CO2和液態水的反應中,每有5NA個電子轉移時,0.5mol乙炔發生反應放出650kJ的熱量,所以2mol乙炔完全反應有20NA個電子轉移時,放出2600kJ的熱量,依據熱化學方程式書寫方法寫出,標注物質聚集狀態和對應反應的焓變.
解答 解:在C2H2(氣態)完全燃燒生成CO2和液態水的反應中,每有5NA個電子轉移時,0.5mol乙炔發生反應放出650kJ的熱量,所以2mol乙炔完全反應有20NA個電子轉移時,放出2600kJ的熱量,則熱化學方程式為:2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=-2600 kJ•mol-1,
故答案為:2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=-2600 kJ•mol-1.
點評 本題考查熱化學方程式的書寫、蓋斯定律、依據氧化還原反應電子轉移計算反應熱等,題目較簡單,注意蓋斯定律的理解與運用.


科目:高中化學 來源: 題型:填空題
| 物質 | CH3OH | CH3OCH3 | H2O |
| 濃度/(mol•L-1) | 0.44 | 0.6 | 0.6 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
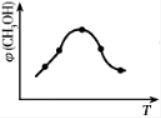
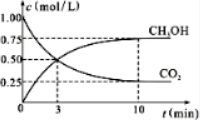
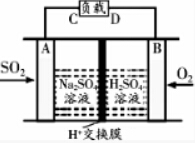
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 已知H2(g)+$\frac{1}{2}$O2(g)═H2O(g);△H=-241.8 kJ•mol-1,則氫氣的燃燒熱為241.8 kJ•mol-1 | |
| B. | 已知C(石墨,s)=C(金剛石,s);△H=+1.9 kJ•mol-1,則石墨比金剛石穩定 | |
| C. | 已知NaOH(aq)+HCl(aq)═NaCl(aq)+H2O(l);△H=-57.3 kJ•mol-1,則含1mol NaOH的稀溶液與1mol的稀醋酸完全中和,放出的熱量也等于57.3kJ | |
| D. | 已知2C(s)+2O2(g)═2CO2(g))△H=a kJ•mol-1、2C(s)+O2(g)═2CO(g)△H=b kJ•mol-1,則a>b |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 2N2H4(g)+2NO2(g)═3N2(g)+4H2O (l)△H=+1135.7kJ•mol-1 | |
| B. | 2N2H4(g)+2NO2(g)═3N2(g)+4H2O(l)△H=-1135.7kJ•mol-1 | |
| C. | N2H4(g)+NO2(g)═$\frac{3}{2}$N2(g)+2H2O(g)△H=+1135.7kJ•mol-1 | |
| D. | 2N2H4(g)+2NO2(g)═3N2(g)+4H2O(g)△H=-1135.7kJ•mol-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 427℃時該反應的平衡常數為9.4,則該反應的△H>0 | |
| B. | 800℃下,該反應的化學平衡常數為0.25 | |
| C. | 同溫下,若繼續向該平衡體系中通入1.0mol的H2O(g),則平衡時H2O(g)轉化率為66.7% | |
| D. | 同溫下,若繼續向該平衡體系中通入1.0mol的CO(g),則平衡時H2O(g)物質的量分數為11.1% |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | H2S+CuSO4═H2SO4+CuS↓ | B. | H2SO4+CuO═CuSO4+H2O | ||
| C. | 2NaOH+CO2═Na2CO3+H2O | D. | Fe2O3+3CO═2Fe+3CO2↑ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com