
| A. | 鋁元素是地殼中含量最多的元素 | |
| B. | 工業煉鋁采用電解熔融的鋁土礦的方法 | |
| C. | 冰晶石能使氧化鋁熔融溫度降低 | |
| D. | 工業上可用電解熔融氯化鋁制取金屬鋁 |
 步步高達標卷系列答案
步步高達標卷系列答案科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用lmol的醋酸溶液和1.01mol的氫氧化鈉溶液做中和熱實驗測得中和熱的數值為57.3kJ/mol | |
| B. | 用25mL滴定管做中和滴定時,用去某濃度的堿溶液21.7mL | |
| C. | 室溫下,用廣泛pH試紙測得某溶液的pH為2.3 | |
| D. | 通過實驗得知在常溫常壓下,12g固體C和32g氣體O2所具有的總能量一定大于44g氣體CO2所具有的總能量 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | pH=3的硝酸跟pH=11的氫氧化鋇溶液 | |
| B. | pH=3的鹽酸跟pH=11的氨水 | |
| C. | pH=3硫酸跟pH=11的氫氧化鈉溶液 | |
| D. | pH=3的醋酸跟pH=11的氫氧化鈉溶液 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫下,將pH=2的鹽酸和pH=12的氨水等體積混合:c(NH4+)>c(Cl-)>c(OH-)>c(H+) | |
| B. | 0.1mol•L-1 Na2CO3溶液:2c(Na+)=c(HCO3-)+c(CO32-)+c(H2CO3) | |
| C. | 相同溫度下,0.6 mol/L氨水溶液與0.3 mol/L氨水溶液中c(OH-)之比是2:1 | |
| D. | 物質的量濃度相等的①NH4HSO4溶液、②NH4HCO3溶液、③NH4Cl溶液中,c(NH4+)的大小關系:①>②>③ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1molFe與足量氯氣充分反應時轉移的電子數為2NA | |
| B. | 18 g水中所含的電子數為10NA | |
| C. | 0.3 mol•L-1Na2SO4溶液中含0.6NA個Na+ | |
| D. | 11.2 L氮氣中含NA個氮原子 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
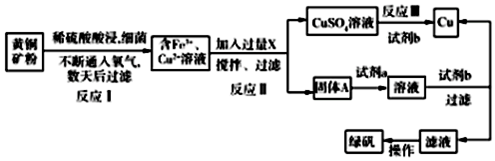
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com