
【題目】在下列各溶液中,指定的離子組一定能大量共存的是( )
A.無色溶液中:K+、Cu2+、Cl-、SO![]()
B.含有0.1mol·L-1Fe3+的溶液中:K+、Mg2+、I-、NO![]()
C.在pH=1的溶液中:K+、Ba2+、Cl-、NO![]()
D.室溫下,![]() =10-13的溶液中:Na+、Fe3+、NO
=10-13的溶液中:Na+、Fe3+、NO![]() 、SO
、SO![]()
科目:高中化學 來源: 題型:
【題目】有MgCl2、Al2(SO4)3的混合溶液,向其中不斷加入NaOH溶液,得到的沉淀量與加入的NaOH溶液的關系如圖所示,則溶液中c(Cl—)與c(SO42—)之比為( )

A. 1∶1 B. 2∶3 C. 3∶2 D. 2∶1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在36 g碳不完全燃燒所得氣體中,CO占![]() 體積,CO2占
體積,CO2占![]() 體積,且C(s)+
體積,且C(s)+![]() O2(g) = CO(g) ΔH=—110.5 kJ/mol;CO(g)+
O2(g) = CO(g) ΔH=—110.5 kJ/mol;CO(g)+![]() O2(g) = CO2(g) ΔH=—283 kJ/mol。與這些碳完全燃燒相比,損失的熱量是 ( )
O2(g) = CO2(g) ΔH=—283 kJ/mol。與這些碳完全燃燒相比,損失的熱量是 ( )
A.172.5 kJB.110.5 kJC.283 kJD.566 kJ
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】明礬石的主要成分是K2SO4·Al2(SO4)3·2Al2O3·6H2O,含有少量氧化鐵,利用明礬石制備K2SO4的工藝流程如圖所示:

據此流程圖回答下列問題:
(1)①焙燒爐中Al2(SO4)3與S反應的產物是兩種氧化物,該反應的化學方程式為______;寫出爐氣的一種用途________。
(2)②中Al2O3參與反應的離子方程式為__________。
(3)③中調節pH不能用CO2的理由是____________________。
(4)工業冶煉金屬鋁需要定期更換補充陽極碳塊的原因是__________________。
(5)純凈氫氧化鋁經歷兩次__________________(填反應類型)可制得鋁。以Al和NiO(OH)為電極,NaOH溶液為電解液組成一種新型電池,放電時NiO(OH)轉化為Ni(OH)2,該電池負極的電極反應式是__________________。
(6)現有明礬石1 625 t,按上述流程制得780 t Al(OH)3,忽略鋁元素的損失,請計算明礬石中鉀元素的質量分數為____________%。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某興趣小組用合金鋁、鐵、銅的廢棄合金為原料制取硝酸銅晶體和氫氧化鋁并測定氫氧化鋁的純度,設計的主要流程如下:

已知:Fe2+沉淀的pH范圍為7.0~9.0;Fe3+沉淀的pH范圍為1.9~3.2;Cu2+沉淀的pH范圍為4.7~6.7。
(1)寫出合金中加入NaOH溶液后所發生的離子反應方程式___,試劑X的名稱為__。
(2)加入Z的作用是調節溶液的pH,pH范圍應為___;下列可作為試劑z的是___。
a.銅粉 b.氨水 c.氧化銅 d.硫酸銅
(3)實驗操作①依次是____、___,過濾洗滌即可得到硝酸銅晶體。
(4)根據流程圖內數據計算:濾渣C中氫氧化鋁的質量分數為___。(用m、n的代數式表示)
(5)按該流程的操作步驟,氫氧化鋁質量分數的測定結果可能性是非常大的,原因有①___;②____。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】T℃時,在1L的密閉容器中充入1molCO2和3molH2,發生反應:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g)H=-49.0kJ·mol-1,測得CO2和CH3OH(g)的濃度隨時間變化曲線如圖所示。下列敘述中,正確的是( )
CH3OH(g)+H2O(g)H=-49.0kJ·mol-1,測得CO2和CH3OH(g)的濃度隨時間變化曲線如圖所示。下列敘述中,正確的是( )
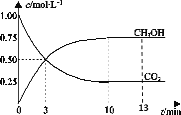
A.T℃時,平衡常數K=3,CO2與H2的平衡轉化率相等
B.T℃時,上述條件下達到平衡時放出49.0kJ的熱量
C.降溫和縮小容器體積均可使反應的平衡常數增大
D.從反應開始到3min,H2的平均反應速率υ(H2)=0.5molL-1min-1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25℃時,向10mL0.10mol·L-1一元弱酸HA(Ka=10-3)中逐滴加入0.10mol·L-1的NaOH溶液,溶液pH隨所加NaOH溶液體積變化如圖。下列說法不正確的是( )
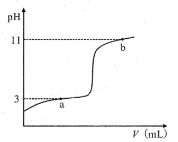
A.a點處存在c(HA)+c(OH-)=c(Na+)+c(H+)
B.b點處存在c(Na+)=c(HA)+c(OH-)+c(A-)
C.由a→b,溶液中n(A-)持續增大
D.V=10mL時,存在c(Na+)>c(A-)>c(OH-)>c(H+)
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】工業上,在催化劑條件下,用NH3作為還原劑將煙氣中的NOx還原成無害的氫氣和水,反應方程式可表示為:2NH3(g)+NO(g)+NO2(g)![]() 2N2(g)+3H2O(g)
2N2(g)+3H2O(g)
(1)一定條件下,在容積為2L的容器內進行該反應,20min時達到平衡,生成N2 0.4mol,則平均反應速率v(NO)=___________________。可從混合氣體的顏色變化判斷上述反應是否達到平衡,其理由是_______________________________________________。
(2)工業上也用氨水吸收SO2尾氣,最終得到(NH4)2SO4,(NH4)2SO4溶液中c(NH4+)與c(SO42-)之比____2:1(選填“>”、“<”、“=”),用離子方程式解釋其原因______________________。
(3)與Cl2相比較,ClO2處理水時被還原成Cl-,不生成有機氯代物等有害物質。工業上可用亞鋁酸鈉和稀鹽酸為原料制備ClO2,反應如下:NaClO2+HCl→ClO2↑+NaCl+_____(沒有配平)
(4)補全方程式并配平,標出電子轉移方向和數目_________________________ 。
(5)該反應中氧化劑和還原劑的物質的量之比是___________。若生成0.2molClO2,轉移電子數為_____個。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】25℃時,用0.1000mol·L-1的鹽酸分別滴定20.00mL 0.1000mol·L-1氨水和20.00mL 0.1000mol·L-1 NaOH溶液,滴定曲線如圖所示。下列說法不正確的是
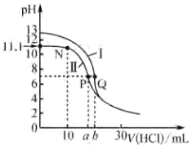
A.25℃,Kb(NH3·H2O)的數量級為10-5
B.N點處的溶液中:c(NH![]() )>c(NH3·H2O)
)>c(NH3·H2O)
C.曲線II滴定終點時所選的指示劑為酚酞
D.Q點所加鹽酸的體積為b mL,則b=20
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com