
| 實驗 編號 | T/K | 催化劑的用量 / g | 酸性KMnO4溶液的濃度/mol·L-1 | 實驗目的 |
| ① | 298 | 0.5 | 0.010 | a. 實驗①和②探究酸性KMnO4溶液的濃度對該反應速率的影響; b. 實驗①和 探究溫度對該反應速率的影響; c. 實驗①和 探究催化劑對該反應速率的影響。 |
| ② | | | | |
| ③ | | | | |
| ④ | | | |
| 實驗編號 | 溶液褪色所需時間 t / min | ||
| 第1次 | 第2次 | 第3次 | |
| ① | 14.0 | 13.0 | 11.0 |
| ② | 6.0 | 7.0 | 7.0 |
| 實驗 編號 | T/K | 催化劑的用量 / g | 酸性KMnO4溶液的濃度/mol·L-1 | 實驗目的 |
| ① | | | | a. 實驗①和②探究酸性KMnO4溶液的濃度對該反應速率的影響; b. 實驗①和③探究溫度對該反應速率的影響; c. 實驗①和④探究催化劑對該反應速率的影響。 |
| ② | 298 | 0.5 | 0.0010 | |
| ③ | 323 | 0.5 | 0.010 | |
| ④ | 298 | 0 | 0.010 |
| 實驗 編號 | T/K | 催化劑的用量 / g | 酸性KMnO4溶液的濃度/mol·L-1 | 實驗目的 |
| ① | | | | a. 實驗①和②探究酸性KMnO4溶液的濃度對該反應速率的影響; b. 實驗①和 ③ 探究溫度對該反應速率的影響; c. 實驗①和 ④ 探究催化劑對該反應速率的影響。 |
| ② | 298 | 0.5 | 0.0010 | |
| ③ | 323 | 0.5 | 0.010 | |
| ④ | 298 | 0 | 0.010 |



科目:高中化學 來源:不詳 題型:單選題
| A.對任何化學反應來說,反應速率越大,反應現象就越明顯 |
| B.化學平衡指化學反應的最大限度,改變條件也不能改變化學平衡 |
| C.可逆反應達到化學平衡狀態時,正、逆反應的速率都為0 |
| D.升高溫度一定能增大反應速率 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 CO(g)+H2O(g)進行甲、乙、丙、丁四組實驗,實驗起始時放入容器內各組分的物質的量見下表
CO(g)+H2O(g)進行甲、乙、丙、丁四組實驗,實驗起始時放入容器內各組分的物質的量見下表 | CO2 | H2 | CO | H2O |
| 甲 | amol | amol | 0mol | 0mol |
| 乙 | 2amol | amol | 0mol | 0mol |
| 丙 | 0mol | 0mol | amol | amol |
| 丁 | amol | 0mol | amol | amol |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
| A.只有②③④ | B.只有②④ | C.只有④ | D.全部 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
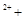 H2O2
H2O2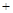 2H
2H → 2Fe
→ 2Fe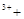 2H2O 2Fe
2H2O 2Fe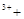 H2O2 → 2Fe
H2O2 → 2Fe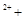 O2↑
O2↑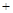 2H
2H
A.H2O2的氧化性比Fe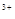 強,其還原性比Fe 強,其還原性比Fe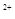 弱 弱 |
| B.在H2O2分解過程中,溶液的pH逐漸下降 |
C.在H2O2分解過程中,Fe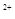 和Fe 和Fe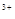 的總量保持不變 的總量保持不變 |
D.H2O2生產過程要嚴格避免混入Fe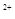 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
 2CO-Q1,反應速率V1;N2+ 3 H2
2CO-Q1,反應速率V1;N2+ 3 H2 2NH3+Q2反應速率V2 。對于上述反應,當溫度升高時,V1和V2的變化情況為( )
2NH3+Q2反應速率V2 。對于上述反應,當溫度升高時,V1和V2的變化情況為( )| A.同時增大 | B.同時減小 |
| C.V1增大,V2減小 | D.V1減小,V2增大 |
查看答案和解析>>
科目:高中化學 來源:不詳 題型:單選題
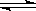 2NH3(g)△H=-92kJ·mol-1下列關于此反應的說法中錯誤的是( )
2NH3(g)△H=-92kJ·mol-1下列關于此反應的說法中錯誤的是( ) | A.加壓可使該反應的反應速率變大 |
| B.升高溫度,該反應的正、逆反應速率均變大 |
| C.將1molN2和3molH2混合進行反應,反應完成時放出的熱量為92kJ |
| D.單位時間內生成1molN2,同時消耗3molH2說明該反應達到平衡狀態 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com