
分析 (1)由題給信息可知Fe2+轉化為Fe3+而中毒,服用維生素C可以解毒,說明在維生素C作用下Fe3+又轉化為Fe2+;
(2)A.亞硝酸鈉是強堿弱酸鹽其水溶液呈堿性,氯化鈉是強酸強堿鹽其水溶液呈中性;
B.酸性條件下,亞硝酸根離子能被碘離子還原生成一氧化氮,同時生成碘單質;
C.甲基橙的變色范圍是3.1-4.4;
D.亞硝酸根離子不和銀離子反應,氯離子和銀離子反應生成白色沉淀;
(3)把新制的氯水加到NaNO2溶液中,觀察到氯水褪色,同時生成NaNO3和HCl,二者發生氧化還原反應,
(4)Cl2、HNO3都能氧化亞鐵離子,但能引入新的雜質,鐵不能氧化亞鐵離子,雙氧水的還原產物是水,不引入雜質;
(5)①根據方程式可知,鐵元素的化合價從+3價升高到+6價,失去3個電子;氯元素的化合價從+1價降低到-1價,得到2個電子,然后根據電子的得失守恒和質量守恒定律配平方程式;
(6)依據高鐵酸根具有強的氧化性,以及反應生成的三價鐵離子能夠水解生成氫氧化鐵膠體的性質解答.
解答 解:(1)服用維生素C可以解毒,說明在維生素C作用下Fe3+又轉化為Fe2+,Fe元素化合價降低,被氧化,則維生素具有還原性,而亞硝酸鹽,會導致Fe2+轉化為Fe3+,說明亞硝酸鹽具有氧化性,在反應中為氧化劑,所以維生素C是還原劑,
故答案為:D;
(2)A.亞硝酸鈉是強堿弱酸鹽其水溶液呈堿性,氯化鈉是強酸強堿鹽其水溶液呈中性,相同物質的量濃度的兩種溶液的pH不同,所以可以用測定這兩種溶液的pH值鑒別,故A不選;
B.在酸性條件下,亞硝酸鈉和碘離子反應方程式為2NO2-+2I-+4H+=2NO↑+I2+2H2O,碘遇淀粉變藍色,氯離子和碘離子不反應,所以反應現象不同,所以可以用酸性條件下的KI淀粉試液來區別,故B不選;
C.亞硝酸鈉是強堿弱酸鹽其水溶液呈堿性,氯化鈉是強酸強堿鹽其水溶液呈中性,甲基橙的變色范圍是3.1-4.4,所以亞硝酸鈉和氯化鈉溶液加入甲基橙后溶液都呈黃色,反應現象相同,所以不能用甲基橙鑒別,故C選;
D.亞硝酸根離子不和銀離子反應,氯離子和銀離子反應生成不溶于硝酸的白色沉淀,反應現象不同,所以可以用AgNO3和HNO3兩種試劑來區別,故D不選;
故答案為:C;
(3)某同學把新制的氯水加到NaNO2溶液中,觀察到氯水褪色,同時生成NaNO3和HCl,反應的離子方程式為:NO2-+Cl2+H2O=NO3-+2H++2Cl-,
故答案為:NO2-+Cl2+H2O=NO3-+2H++2Cl-;
(4)由于Cl2、HNO3都能氧化亞鐵離子,但能引入新的雜質,鐵不能氧化亞鐵離子,雙氧水的還原產物是水,不引入雜質,所以正確是雙氧水,
故答案為:C;
(5)①根據方程式可知,鐵元素的化合價從+3價升高到+6價,失去3個電子;氯元素的化合價從+1價降低到-1價,得到2個電子,氯元素反應化合價降低2價,最小公倍數是6,所以硝酸鐵前面配2,NaClO前面配3,再根據質量守恒配平其他物質,配平后的方程式為:3NaClO+2Fe(NO3)3+10NaOH=2Na2FeO4↓+3NaCl+6NaNO3+5H2O,故答案為:3、2、10、2、3、6、5H2O;
(6)高鐵酸鉀( K2FeO4)中Fe的化合價是+6價,具有強氧化性,能殺菌消毒,其還原產物Fe3+水解生成氫氧化鐵膠體,能吸附水中雜質,所以高鐵酸鉀作為水處理劑發揮的作用是凈水、殺菌消毒;
故答案為:凈水;殺菌消毒.
點評 本題考查綜合考查鐵鹽和亞鐵鹽的相互轉化,亞硝酸鹽的性質,注意二價鐵離子和三價鐵離子的檢驗是高考的熱點,涉及了化學方程式的配平,為高頻考點,側重于學生的分析能力的考查,注意相關基礎知識的積累,難度不大.


科目:高中化學 來源:2016-2017學年河北省唐山市高二上10月月考化學試卷 (解析版) 題型:選擇題
近來科學家研制了一種新型的乙醇電池(DEFC),它用磺酸類質子作溶劑,在200℃左右時供電,乙醇電池比甲醇電池效率高出32倍且更加安全。電池總反應式為
C2H5OH+3O2===2CO2+3H2O,下列說法不正確的是( )
A.C2H5OH在電池的負極上參加反應
B.1 mol乙醇被氧化轉移6 mol電子
C.在外電路中電子由負極沿導線流向正極
D.電池正極的電極反應為4H++O2+4e-===2H2O
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
 | ① | ② | ③ | ④ | ⑤[ | ⑥ | ⑦ | ⑧ |
| 原子半徑/10-10m | 0.66 | 1.36 | 1.23 | 1.10 | 0.99 | 1.54 | 0.70 | 1.18 |
| 最高正化合價 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| 負化合價 | -2 | -3 | -1 | -3 |
| A. | 元素①⑧形成的化合物具有兩性 | |
| B. | 元素⑦位于第二周期Ⅴ族 | |
| C. | 元素④⑤形成的化合物是離子化合物 | |
| D. | 元素⑥的最高價氧化物對應水化物堿性最強 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 進行硫酸銅溶液的濃縮結晶實驗需要的儀器主要有燒杯、玻璃棒、蒸發皿 | |
| B. | 用容量瓶配溶液時,若加水超過刻度線,立即用滴管吸出多余液體 | |
| C. | 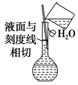 按圖所示配制溶液 | |
| D. | 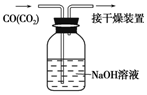 按如圖可除去CO中混有的CO2 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
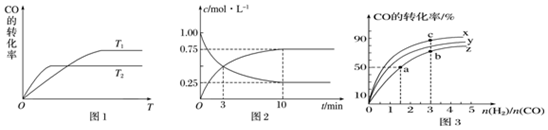
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 食鹽水、牛奶、豆漿 | B. | 碘酒、泥水、血液 | ||
| C. | 白糖水、食鹽水、茶葉水 | D. | Ca(OH)2懸濁液、澄清石灰水、石灰漿 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
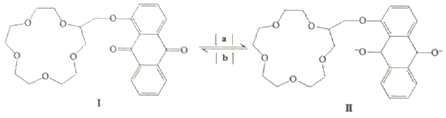
| A. | 物質Ⅰ的分子式是C25H28O8 | B. | 反應是氧化反應 | ||
| C. | 1molⅠ可與8molH2發生加成反應 | D. | 物質Ⅰ的所有原子不可能共平面 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com