
【題目】amol FeS與bmol FeO投入到VL、c mol/L的硝酸溶液中充分反應產生NO氣體,所得澄清溶液成分可看作是Fe(NO3)3、H2SO4的混合液,則反應中未被還原的硝酸可能為
( )
①(a+b)×63g ②(a+b)×189g ③(a+b)mol ④![]() mol
mol
A.①④B.②③C.①③D.②④
 世紀百通期末金卷系列答案
世紀百通期末金卷系列答案科目:高中化學 來源: 題型:
【題目】現對三種不同的鎂鋁合金樣品進行編號,做以下實驗探究。
(1)取樣品①m1g,加入過量NaOH溶液,充分反應后過濾;往濾液中通入過量CO2氣體:將所得沉淀過濾、洗滌、烘干,灼燒,得到固體的質量仍然為m1g.合金中鎂的質量分數為_____(保留2位小數,下同)。
(2)取樣品②m2g,與足量稀硫酸反應,固體完全溶解時得到氣體的體積為VL(標準狀況)。m2的取值范圍是_____。
(3)取樣品③0.918g與30.00mL、2.00mL鹽酸充分反應后,得到672mL氣體(標準狀況)。剩余合金0.306g(認為合金中鎂、鋁與酸的反應同時發生)。然后在反應后所得體系中繼續加1.00mol/L的NaOH溶液,恰好使所有鋁元素均不以沉淀形式存在。則需要加入1.00mol/L的NaOH溶液_____mL。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知反應:2NO(g)+Br2(g)![]() 2NOBr(g) △H=-a kJ·mol-1 (a>0),其反應機理如下
2NOBr(g) △H=-a kJ·mol-1 (a>0),其反應機理如下
①NO(g)+Br2(g)![]() NOBr2(g) 快 ②NO(g)+NOBr2(g)
NOBr2(g) 快 ②NO(g)+NOBr2(g)![]() 2NOBr(g) 慢
2NOBr(g) 慢
下列有關該反應的說法正確的是( )
A. 該反應的速率主要取決于①的快慢
B. NOBr2是該反應的催化劑
C. 正反應的活化能比逆反應的活化能小a kJ·mol-1
D. 增大Br2(g)濃度能增大活化分子百分數, 加快反應速率
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在溫度T1和T2時,分別將0.50 mol CH4和1.2mol NO2充入1 L的密閉容器中發生反應:
CH4(g)+2NO2(g)![]() N2(g)+CO2(g)+2H2O(g)△H=akJ/mol。測得有關數據如下表:
N2(g)+CO2(g)+2H2O(g)△H=akJ/mol。測得有關數據如下表:
溫度 | 時間/min 物質的量 | 0 | 10 | 20 | 40 | 50 |
T1 | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
T2 | n(CH4)/mol | 0.50 | 0.30 | 0.18 | x | 0.15 |
下列說法正確的是
A.T1>T2,且a>0
B.當溫度為T2、反應進行到40 min時, x>0.15
C.溫度為T2時,若向平衡后的容器中再充入0.50 mol CH4和1.2mol NO2,重新達到平衡時,n(N2)=0.70mol
D.溫度為T1時,達平衡時CH4 的轉化率大于NO2的轉化率
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室探究SO2與Fe(NO3)3溶液反應的原理,裝置如下圖,實驗中Y裝置產生白色沉淀。下列說法不正確的是
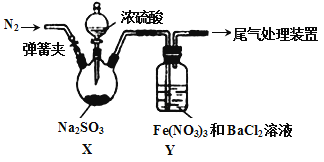
A. 滴加濃硫酸之前應進行的操作是打開彈簧夾,通入一段時間N2
B. Y中產生的白色沉淀是BaSO4或BaSO3
C. 產生白色沉淀的原因可能是在酸性條件下SO2與NO3- 反應生成了SO42-
D. 若將Fe(NO3)3換成FeCl3,Y中也能產生白色沉淀,說明Fe3+也能將SO2氧化
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為驗證氯、溴、碘三種元素的非金屬性強弱,用下圖所示裝置進行試驗(夾持儀器已略去,氣密性已檢驗)。
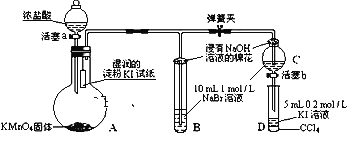
實驗過程:
①打開彈簧夾,打開活塞a,滴加濃鹽酸。
②當B和C中的溶液都變為黃色時,夾緊彈簧夾。
③當B中溶液由黃色變為棕紅色時,關閉活塞a。
④……
(1)A中發生反應生成氯氣,該反應的離子方程式為_____________。
(2)驗證氯氣的氧化性強于碘的實驗現象是__________________。
(3)B、C管口“浸有NaOH溶液的棉花”的作用是______________。
(4)為驗證溴的氧化性強于碘,過程④的操作和現象是____________。
(5)過程③實驗的目的是____________。
(6)運用原子結構理論解釋氯、溴、碘非金屬性逐漸減弱的原因是_______________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】煙氣的脫硝(除![]() )技術和脫硫(除
)技術和脫硫(除![]() )技術都是目前環境科學研究的熱點。
)技術都是目前環境科學研究的熱點。
(1)工業上可以采用“質子膜電解槽”對煙氣進行脫硫脫硝,其工藝如圖甲所示:
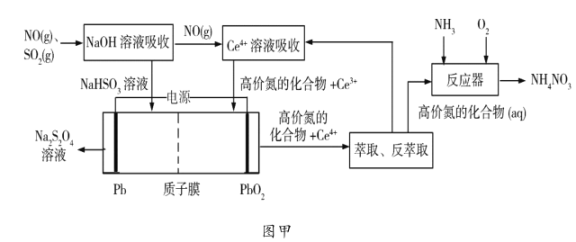
①![]() 溶液吸收
溶液吸收![]() 主要反應的化學方程式為___________;
主要反應的化學方程式為___________;
②電解的主要目的是______________,陰極的電極反應式為______________;
③“高價氮的化合物”中NO2在反應器中發生化合反應的化學方程式為______;
(2)利用活性焦炭的吸附作用,可以對煙氣進行脫硫和脫硝。被吸附的![]() 與活性焦炭反應生成
與活性焦炭反應生成![]() 和
和![]() ,當生成
,當生成![]() 時,轉移電子的物質的量為__________
時,轉移電子的物質的量為__________![]() ;
;
(3)一定條件下,將一定濃度NOx(NO2和NO的混合氣體)通入![]() 的
的![]() 乳濁液中,發生的反應如下:
乳濁液中,發生的反應如下:![]() ,
,![]() ,改變
,改變![]() ,
,![]() 的去除率變化情況如圖乙所示。
的去除率變化情況如圖乙所示。
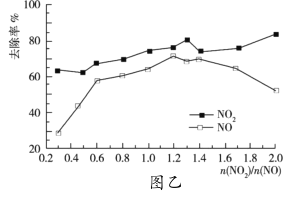
①當![]() 大于1.4時,
大于1.4時,![]() 去除率升高,但
去除率升高,但![]() 的去除率卻降低。其可能的原因是__;
的去除率卻降低。其可能的原因是__;
②![]() 和
和![]() 發生的主要反應為
發生的主要反應為![]() 。保持
。保持![]() 的初始濃度不變,改變
的初始濃度不變,改變![]() ,將反應后的混合氣體通入
,將反應后的混合氣體通入![]() 乳濁液中吸收。為節省
乳濁液中吸收。為節省![]() 的用量,又能保持
的用量,又能保持![]() 去除效果,則
去除效果,則![]() 合適的值約為___________;
合適的值約為___________;
(4)已知:![]() ,
,![]() ,則
,則![]() ______________________。
______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】固體氧化物燃料電池是由美國西屋(Westinghouse)公司研制開發的。它以固體氧化鋯—氧化釔為電解質,這種固體電解質在高溫下允許氧離子(O2-)在其間通過。該電池的工作原理如下圖所示,其中多孔電極a、b均不參與電極反應。下列判斷正確的是

A. 有O2放電的a極為電池的負極
B. O2-移向電池的正極
C. b極對應的電極反應為2H2-4e-+2O2-=2H2O
D. a極對應的電極反應為O2+2H2O+4e-=4OH-
查看答案和解析>>
科目:高中化學 來源: 題型:
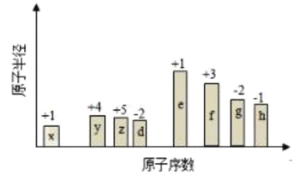
【題目】隨原子序數的遞增,八種短周期元素的原子半徑的相對大小、最高正價或最低負價的變化如下圖所示,下列分析正確的是( )
A.![]() 、
、![]() 的簡單離子半徑大小:
的簡單離子半徑大小:![]()
B.元素的金屬性:![]()
C.元素的非金屬性:![]()
D.![]() 、
、![]() 、
、![]() 和
和![]() 四種元素能形成離子化合物
四種元素能形成離子化合物
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com