
| A. | 失電子的反應 | B. | 原電池的正極反應 | ||
| C. | 放熱反應 | D. | 電鍍池鍍件一極的反應 |
科目:高中化學 來源: 題型:選擇題
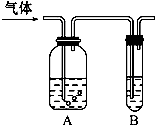 如圖把氣體緩慢通過盛有足量試劑的試劑瓶A,在試管B中可以觀察到明顯現象的是( )
如圖把氣體緩慢通過盛有足量試劑的試劑瓶A,在試管B中可以觀察到明顯現象的是( )| 選項 | 氣怵 | A中試剤 | B中試剤 |
| A | SO2、CO2 | 酸性KMnO4溶液 | 品紅溶液 |
| B | Cl2、HC1 | 濃硫酸 | KI淀粉溶液 |
| C | NH3、CO2 | 濃硫酸 | 酚酞試液 |
| D | CO2、HC1 | NaOH溶液 | 澄清石灰水 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | NA個氧氣分子和NA個氫氣分子的質量比為16:1 | |
| B. | 54g H2O中含有的水分子數為3NA個 | |
| C. | 11.2L 氯氣中含有的原子數為NA個 | |
| D. | 2L 1mol/L Na2SO4溶液中Na+離子數為2NA個 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
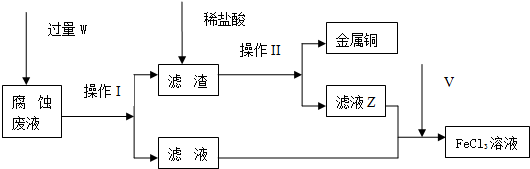
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1 L 1 mol•L-1的NaClO溶液中含有ClO-的數目為NA | |
| B. | 78 g苯含有CC雙鍵的數目為3NA | |
| C. | 常溫常壓下,14 g由N2與CO組成的混合氣體含有的原子數目為NA | |
| D. | 標準狀況下,6.72 L NO2與水充分反應轉移的電子數目為0.1NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 10 (b-2a)mol•L-1 | B. | 5(b-2a)mol•L-1 | C. | 2(b-a)mol•L-1 | D. | 10(2a-b)mol•L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題

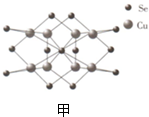

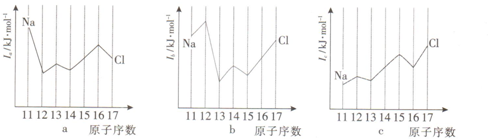
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com