
NOx是汽車尾氣中的主要污染物之一。
(1)NOx能形成酸雨,寫出NO2轉化為HNO3的化學方程式:__________________________。
(2)汽車發動機工作時會引發N2和O2反應,其能量變化示意圖如下:
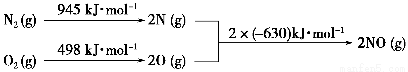
①寫出該反應的熱化學方程式:_______________________________。
②隨溫度升高,該反應化學平衡常數的變化趨勢是____。
(3)在汽車尾氣系統中裝置催化轉化器,可有效降低NOx的排放。
①當尾氣中空氣不足時,NOx在催化轉化器中被還原成N2排出。寫出NO被CO還原的化學方程式:______________________________
②當尾氣中空氣過量時,催化轉化器中的金屬氧化物吸收NOx生成鹽。其吸收能力順序如下:12MgO<20CaO<38SrO<56BaO。原因是___________________________________________,
元素的金屬性逐漸增強,金屬氧化物對NOx的吸收能力逐漸增強。
(4)通過NOx傳感器可監測NOx的含量,其工作原理示意圖如下:

①Pt電極上發生的是________反應(填“氧化”或“還原”)
②寫出NiO電極的電極反應式:______________________________________。
(1)3NO2+H2O=2HNO3+NO
(2)①N2(g)+O2(g)=2NO(g) ΔH=+183 kJ·mol-1 ②增大
(3)①2CO+2NO N2+2CO2
N2+2CO2
②根據Mg、Ca、Sr和Ba的質子數,得知它們均為ⅡA族元素。同一主族的元素,從上到下,原子半徑逐漸增大
(4)①還原 ②NO+O2--2e-=NO2
【解析】(1)NO2轉化為HNO3的化學方程式為:3NO2+H2O=2HNO3+NO。
(2)①拆開化學鍵吸收能量,形成化學鍵釋放能量
N2(g)+O2(g)=2NO(g)其ΔH計算方法如下
ΔH=945 kJ·mol-1+498 kJ·mol-1-2×630 kJ·mol-1=+183 kJ·mol-1
②該反應為吸熱反應,升高溫度,化學平衡向正反應方向移動,化學平衡常數增大。
(3)①NO和CO發生反應生成N2和CO2,其化學方程式為2CO+2NO N2+2CO2。
N2+2CO2。
②分析12MgO<20CaO<38SrO<56BaO的排列順序,不難發現上述四種氧化物對應金屬元素為ⅡA族元素,且質子數依次增大,電子層數依次增多,原子半徑依次增大,元素的金屬性逐漸增強,結合元素周期表的知識,作出合理的解釋。
(4)由圖示可知發生原電池反應為2NO+O2=2NO2,NO為還原劑,O2為氧化劑,O2在Pt電極電子發生還原反應:O2+4e-=2O2-。NO在NiO電極上失電子發生氧化反應:NO+O2--2e-=NO2。


科目:高中化學 來源:2013-2014學年高考化學二輪復習必做訓練 化學基本概念練習卷(解析版) 題型:填空題
中學常見的某反應的化學方程式為a+b―→c+d+H2O(未配平,反應條件已略去)。
請回答下列問題:
(1)若a是鐵,b是稀硝酸(過量),且a可溶于c溶液中。則a與b反應的離子方程式為
___________________________。
(2)若c、d為氣體,且都能使澄清石灰水變渾濁,則將此混合氣體通入溴水中,橙色褪去,寫出其褪色過程中發生反應的離子方程式:___________________________。
(3)若c是無色有刺激性氣味的氣體,其水溶液顯弱堿性,在標準狀況下用排空氣法收集c氣體,得平均摩爾質量為20 g·mol-1的混合氣體進行噴泉實驗。假設溶質不擴散,實驗完成后燒瓶中所得溶液的物質的量濃度為________mol·L-1(小數點后保留2位有效數字)。
(4)若a是造成溫室效應的主要氣體,c、d均為鈉鹽,參加反應的a、b的物質的量之比為4:5。則上述反應的離子方程式為____________________________。
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習必做訓練 化學與技術練習卷(解析版) 題型:選擇題
工業上利用H2在Cl2中燃燒,所得產物再溶于水的方法制得鹽酸,流程復雜且造成能量浪費。有人設想利用原電池原理直接制備鹽酸的同時,獲取電能,假設這種想法可行,下列說法肯定錯誤的是( )
A.兩極材料都是石墨,用稀鹽酸作電解質溶液
B.通入氫氣的電極為原電池的正極
C.電解質溶液中的陽離子向通入氯氣的電極移動
D.通氯氣的電極反應為Cl2+2e-=2Cl-
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習必做訓練 元素及其化合物練習卷(解析版) 題型:選擇題
新課程倡導合作學習和探究學習。科學的假設與猜想是科學探究的前提,在下列假設(猜想)引導下的探究肯定沒有意義的選項是( )
A.探究SO2和Na2O2反應可能有Na2SO4生成
B.探究Na與水的反應生成的氣體可能是O2
C.探究濃硫酸與銅在一定條件下反應產生的黑色物質可能是CuO
D.探究向滴有酚酞試液的NaOH溶液中通入Cl2,酚酞紅色褪去的現象是溶液的酸堿性改變所致,還是HClO的漂白性
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習必做訓練 元素及其化合物練習卷(解析版) 題型:選擇題
下列各組物質中,物質之間通過一步反應就能實現圖示變化的是( )
物質 編號 | 物質轉化關系 | a | b | c | d |
① |
| FeCl2 | FeCl3 | Fe | CuCl2 |
② | NO | NO2 | N2 | HNO3 | |
③ | Na2O | Na2O2 | Na | NaOH | |
④ | Al2O3 | NaAlO2 | Al | Al(OH)3 |
A.①④ B.②③ C.①③ D.②④
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習四川配套訓練 第9講非金屬元素化合物練習卷(解析版) 題型:選擇題
甲、乙、丙、丁四種物質中,甲、乙、丙均含有相同的某種元素,它們之間具有如下轉化關系:  丙。下列有關物質的推斷不正確的是( )。
丙。下列有關物質的推斷不正確的是( )。
A.若甲為焦炭,則丁可能是O2
B.若甲為SO2,則丁可能是氨水
C.若甲為Fe,則丁可能是鹽酸
D.若甲為NaOH溶液,則丁可能是CO2
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習四川配套訓練 第8講電化學練習卷(解析版) 題型:填空題
新型鋰離子電池材料Li2MSiO4(M為Fe,Co,Mn,Cu等)是一種發展潛力很大的電池電極材料。工業制備Li2MSiO4有兩種方法。
方法一:固相法,2Li2SiO3+FeSO4 Li2FeSiO4+Li2SO4+SiO2。
Li2FeSiO4+Li2SO4+SiO2。
方法二:溶膠-凝膠法,CH3COOLi、Fe(NO3)3、Si(OC2H5)4等試劑 膠體
膠體 干凝膠
干凝膠 Li2FeSiO4。
Li2FeSiO4。
(1)固相法中制備Li2FeSiO4過程采用惰性氣體氣氛,其原因是
______________________________________________________________________。
(2)溶膠?凝膠法中,檢查溶液中有膠體生成的方法是________;生產中,生成1 mol Li2FeSiO4整個過程轉移電子的物質的量為________mol。
(3)以Li2FeSiO4和嵌有Li的石墨為電極材料,含鋰的導電固體作電解質,構成電池的總反應式為Li+LiFeSiO4 Li2FeSiO4,則該電池的負極是________;充電時,陽極反應的電極反應式為________。
Li2FeSiO4,則該電池的負極是________;充電時,陽極反應的電極反應式為________。
(4)使用(3)組裝的電池必須先________。
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習四川配套訓練 第7講水溶液中的離子平衡練習卷(解析版) 題型:選擇題
下列說法正確的是( )。
A.0.1 mol·L-1的醋酸溶液加水稀釋,  減小
減小
B.體積、pH均相同的醋酸和鹽酸完全溶解等量的鎂粉(少量),后者用時少
C.向水中加入少量固體硫酸氫鈉,c(H+)增大,KW變大
D.常溫下,V1 L pH=11的NaOH溶液與V2 L pH=3的HA溶液混合,若混合液顯中性,則V1≤V2
查看答案和解析>>
科目:高中化學 來源:2013-2014學年高考化學二輪復習四川配套訓練 第3講兩種重要的反應練習卷(解析版) 題型:選擇題
下列對各組離子或物質是否能夠大量共存解釋正確的是( )。
A常溫常壓下NH3、O2、H2、CO2不能共存NH3為堿性氣體、CO2為酸性氣體,二者反應生成(NH4)2CO3
Bc(OH-)=1.0×10-13 mol·L-1溶液中,Fe2+、NO3—、SO42—、Na+不能共存 發生反應:3Fe2++NO3—+4H+=3Fe3++NO↑+2H2O
C溶液中:K+、Cu2+、Cl-、NH3·H2O不能共存發生反應:Cu2++2OH-=Cu(OH)2↓
D溶液中:Al3+、Na+、SO42—、HCO3—可以共存不能發生反應
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com