
【題目】有機物 X(C4H6O5)廣泛存在于許多水果內,尤以葡萄、西瓜、山渣內為多,X 的碳鏈結構無支鏈,分子式為 C4H6O5;1.34gX 與足量的鈉溶液反應,生成標準狀況下的氣體 0.336L。X與醇或羧酸在濃 H2SO4 和加熱的條件下均生成有香味的產物。X 在一定條件下可發生反應生成A,A![]() B
B![]() C(X、A、B、C 分子中碳原子數目相同)。下列有關說法中不正確的是( )
C(X、A、B、C 分子中碳原子數目相同)。下列有關說法中不正確的是( )
A.X 的結構簡式為 HOOC—CHOH—CH2—COOH
B.A 的分子式為 C4H4O4
C.與 X的官能團種類、數量完全相同的同分異構體還有 3 種
D.C 物質能溶于水
【答案】C
【解析】
X的分子式為C4H6O5,1.34gX與足量的鈉反應,生成標準狀況下的氣體 0.336L,則n(X)=![]() =0.01mol,n(H2)=
=0.01mol,n(H2)=![]() =0.015mol;X分子式為C4H6O5,不飽和度為
=0.015mol;X分子式為C4H6O5,不飽和度為![]() =2,X與醇(ROH)或羧酸(RCOOH)在濃H2SO4和加熱條件下均可反應生成有香味的產物,則X含有羥基、羧基,X在一定條件下的分子內脫水產物A可和溴水發生加成反應,所以X發生醇的消去反應,1molX與足量的金屬鈉反應產生1.5molH2,X分子中可能有一個羥基和二個羧基,X的碳鏈結構無支鏈,X的結構簡式為:HOOCCH(OH)CH2COOH;所以A的結構簡式為HOOC—CH=CH—COOH,B為HOOC-CHBr-CHBr-COOH,C為NaOOC-CHOH-CHOH-COONa,據此進行判斷。
=2,X與醇(ROH)或羧酸(RCOOH)在濃H2SO4和加熱條件下均可反應生成有香味的產物,則X含有羥基、羧基,X在一定條件下的分子內脫水產物A可和溴水發生加成反應,所以X發生醇的消去反應,1molX與足量的金屬鈉反應產生1.5molH2,X分子中可能有一個羥基和二個羧基,X的碳鏈結構無支鏈,X的結構簡式為:HOOCCH(OH)CH2COOH;所以A的結構簡式為HOOC—CH=CH—COOH,B為HOOC-CHBr-CHBr-COOH,C為NaOOC-CHOH-CHOH-COONa,據此進行判斷。
A.由上述分析可以知道,X 的結構簡式為 HOOC—CHOH—CH2—COOH,故A正確;
B. 由上述分析可以知道,X 的結構簡式為 HOOC—CHOH—CH2—COOH ,X發生消去生成A,所以A的結構簡式為HOOC—CH=CH—COOH,所以A的分子式為C4H4O4,故 B正確;
C.與X的官能團種類、數量完全相同的同分異構體還有(HOOC)2CH-CH2OH、(HOOC)2COH-CH32種,故C錯誤;
D. 由上述分析可以知道,C為NaOOC-CHOH-CHOH-COONa,羧基鹽溶于水,羥基為親水基,所以C能溶于水,故D正確。
故答案選C。


科目:高中化學 來源: 題型:
【題目】設阿伏加德羅常數的值為![]() 。下列說法正確的是
。下列說法正確的是
A.![]() 氧氣與
氧氣與![]() 金屬鈉充分反應,轉移的電子數為
金屬鈉充分反應,轉移的電子數為![]()
B.加熱時,![]() 銅粉與足量濃硫酸反應,轉移的電子數為
銅粉與足量濃硫酸反應,轉移的電子數為![]()
C.將![]() 乙烷和
乙烷和![]() 混合光照,生成一氯乙烷的分子數為
混合光照,生成一氯乙烷的分子數為![]()
D.![]() 的
的![]() 溶液中
溶液中![]() 的數目小于
的數目小于![]()
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】為了證明在實驗室制備得到的Cl2中會混有HCl,甲同學設計了如圖所示的實驗裝置,按要求回答下列問題。

(1)請根據甲同學的示意圖,所需實驗裝置從左至右的連接順序:裝置②→__________。
(2)裝置②中主要玻璃儀器的名稱__________、__________、__________。
(3)實驗室制備Cl2的離子方程式為____________。
(4)裝置③中Cu的作用__________(用化學方程式表示)。
(5)乙同學認為甲同學實驗設計仍然存在缺陷,不能證明最終通入AgNO3溶液中的氣體只有一種。為此,乙同學提出氣體通入裝置①之前,要加裝一個檢驗裝置⑤,以證明最終通入AgNO3溶液中的氣體只有一種。你認為裝置⑤應放入__________。
(6)丙同學看到甲同學設計的裝置后提出無需多加裝置,只需將原來燒杯中的AgNO3溶液換成紫色石蕊試液,如果觀察到__________的現象,則證明制Cl2時有HCl揮發出來。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】室溫下,用滴定管量取一定體積的濃氯水置于錐形瓶中,用NaOH溶液以恒定速度來滴定該濃氯水,根據測定結果繪制出ClO-、ClO3-等離子的物質的量濃度c與時間t的關系曲線如下。下列說法正確的是( )

A.NaOH溶液和濃氯水可以使用同種滴定管盛裝
B.a點溶液中存在如下關系:c(Na+) + c(H+) = c(ClO-)+ c(OH-)+ c(ClO3-)
C.b點溶液中各離子濃度:c(Na+) > c(Cl-) > c(ClO-) = c(ClO3-)
D.t2~t4,ClO-的物質的量下降的原因可能是ClO-自身歧化:2ClO-= Cl-+ ClO3-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】如下圖所示,圖Ⅰ是恒壓密閉容器,圖Ⅱ是恒容密閉容器。當其它條件相同時,在Ⅰ、Ⅱ中分別加入2mol![]() 和2mol
和2mol![]() ,開始時容器的體積均為VL,發生如下反應并達到平衡狀態
,開始時容器的體積均為VL,發生如下反應并達到平衡狀態![]() 提示:物質X,Y的狀態均未知,物質Z的狀態為氣態),2X(?)+Y(?)
提示:物質X,Y的狀態均未知,物質Z的狀態為氣態),2X(?)+Y(?)![]() aZ(g)此時Ⅰ中X,Y,Z的物質的量之比為1:3:2。下列判斷正確的是
aZ(g)此時Ⅰ中X,Y,Z的物質的量之比為1:3:2。下列判斷正確的是![]()
![]()
Ⅰ Ⅱ
Ⅱ Ⅲ
Ⅲ
A.物質Z的化學計量數 a= 2
B.若X、Y均為氣態,則在平衡時X的轉化率:Ⅰ<Ⅱ
C.若Ⅱ中氣體的密度如圖Ⅲ所示,則X、Y中只有一種為氣態
D.若X為固態、Y為氣態,則Ⅰ、Ⅱ中從開始到平衡所需的時間:Ⅰ>Ⅱ
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】鋁土礦主要成分Al2O3,還含少量 SiO2、Fe2O3雜質。可用下圖制備鋁:
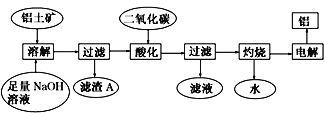
已知 2Na2SiO3+2NaAlO2+2H2O === Na2Al2Si2O8↓+4NaOH。 回答下列問題:
(1)在工藝流程第五步中,灼燒所需的實驗儀器除酒精燈、坩堝、坩堝鉗、玻璃棒之外,還需要_____________、_________________________。
(2)Na2Al2Si2O8的氧化物形式為_________________________。
(3)濾渣A經多步可制得粗硅 ,請寫出由二氧化硅制得粗硅的化學方程式________________。
(4)在工藝流程第三步中,通入過量的二氧化碳時,該反應的離子方程式有_______________, 得到的濾液與足量Ba(OH)2溶液反應的主要離子方程式為 ____________________。
(5)將a g鋁土礦經過以上一系列操作之后,最終得到b g Al(不考慮實驗過程中操作引起的損耗), 下列說法正確的是____________。 (NA表示阿伏加德羅常數)
A.鋁土礦中 Al3+數目小于![]()
B.鋁土礦中Al2O3物質的量小于b/54 mol
C.鋁土礦中鋁元素的質量分數為![]() ×100℅
×100℅
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】H3BO3可以通過電解NaB(OH)4溶液的方法制備,其工作原理如圖,下列敘述錯誤的是( )

A. M室發生的電極反應式為:2H2O-4e- = O2↑+4H+
B. N室中:a% <b%
C. b膜為陰膜,產品室發生反應的化學原理為強酸制弱酸
D. 理論上每生成1mol產品,陰極室可生成標準狀況下5.6L氣體
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】向50 mL稀H2SO4與稀HNO3的混合溶液中逐漸加入鐵粉,假設加入鐵粉的質量與產生氣體的體積(標準狀況)之間的關系如圖所示,且每一段只對應一個反應。下列說法正確的是( )

A. 開始時產生的氣體為H2
B. AB段發生的反應為置換反應
C. 參加反應鐵粉的總質量m2=5.6 g
D. 所用混合溶液中c(HNO3)=0.5 molL﹣1
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】N2與H2反應生成NH3的過程中能量變化曲線如圖所示。若在一個固定容積的密閉容器中充入1 mol N2和3 mol H2,使反應N2+3H2![]() 2NH3達到平衡,測得反應放出熱量為Q1。
2NH3達到平衡,測得反應放出熱量為Q1。
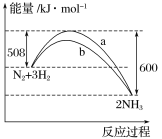
(1)該反應的熱化學方程式為__________________________。
(2)Q1________92 kJ(填“>”“<”或“=”)。
(3)曲線a和曲線b中,加了催化劑的是________。
(4)上述反應達到平衡后,升高溫度H2的轉化率________(填“增大”“不變”或“減小”)。
(5)在溫度體積一定的條件下,若通入2 mol N2和6 mol H2反應后放出的熱量為Q2 kJ,則2Q1與Q2的關系為: Q2 ______2Q1(“>”、“=”或“<”)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com