
【題目】 是一種重要的化工原料,下列有關說法錯誤的是( )
是一種重要的化工原料,下列有關說法錯誤的是( )
A.該物質的分子式為C7H8O
B.該物質屬于芳香族化合物的同分異構體共有4種(不包括其本身)
C.該分子中所有碳原子共平面
D.1 mol該物質與足量的Na反應可產生11.2 L H2
科目:高中化學 來源: 題型:
【題目】實驗室用濃度為0.500mol/L的標準氫氧化鈉溶液來測定未知濃度的鹽酸。在錐形瓶中放入20.00mL的待測溶液,再滴加2滴酚酞,搖勻。用標準氫氧化鈉溶液滴定,直到滴入最后一滴氫氧化鈉溶液,指示劑的顏色_______,并在半分鐘內溶液顏色不發生變化,停止滴定,記錄讀數。數據如表:
次數 | 滴定前(mL) | 滴定后(mL) |
1 | 0.40 | 21.10 |
2 | 0.10 |
第2次滴定后滴定管的讀數如圖所示。根據表中的數據計算出鹽酸的濃度為_____mol/L。

查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】汽車尾氣和燃煤尾氣是造成霧霾的主要原因之一。
(1)工業上利用甲烷催化還原NO,可減少氮氧化物的排放。
已知:CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH=-574kJ·mol1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH =-1160kJ·mol1
甲烷直接將NO2還原為N2的熱化學方程式為____________________________。
(2)減少汽車尾氣污染的原理為2NO(g)+2CO(g)![]() N2(g)+2CO2(g) ΔH <0。向恒溫恒容密閉容器中充入NO和CO,用傳感器測得的數據如下表所示:
N2(g)+2CO2(g) ΔH <0。向恒溫恒容密閉容器中充入NO和CO,用傳感器測得的數據如下表所示:
時間/s | 0 | 1 | 2 | 3 | 4 |
c(NO)/×10-3mol·L1 | 9.00 | 4.00 | 2.00 | 1.00 | 1.00 |
c(CO)/×10-3mol·L1 | 9.00 | 4.00 | 2.00 | 1.00 | 1.00 |
①為了提高尾氣處理的效果,可采取的措施有____________(寫出兩種即可)。
②此條件下達到平衡時,計算該反應的平衡常數K=____________________。
(3)工業上用氫氧化鈉溶液來同時吸收SO2和氮的氧化物氣體(NOx),可得到Na2SO3、NaHSO3、NaNO2、NaNO3等溶液。(已知:常溫下,HNO2的電離常數為Ka=7×10-4,H2SO3的電離常數為Ka1=1.2×10-2、Ka2=5.8×10-8)。
①常溫下,相同濃度的Na2SO3、NaNO2溶液中pH較大的是________溶液。
②常溫下,NaHSO3顯_________性(填“酸”“堿”或“中”),判斷的理由是________________________________________________(通過計算說明)。
(4)鈰素(Ce)常見有+3、+4兩種價態。NO可以被含Ce4+的溶液吸收,生成NO2-、NO3-(二者物質的量之比為1∶1)。可采用電解法將上述吸收液中的NO2-轉化為無毒物質,同時再生Ce4+,其原理如圖所示。

①Ce4+從電解槽的__________(填字母代號)口流出。
②寫出陰極的電極反應式______________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某有機物的結構簡式如圖所示,下列說法中不正確的是( )
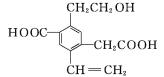
A.1 mol該有機物和過量的金屬鈉反應最多可以生成1.5 mol H2
B.該有機物最多消耗Na、NaOH、NaHCO3的物質的量之比為3∶2∶2
C.可以用酸性KMnO4溶液檢驗其中的碳碳雙鍵
D.該有機物能夠在催化劑作用下發生酯化反應
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】研究表明,氮氧化物和二氧化硫在形成霧霾時與大氣中的氨有關(如下圖所示)。下列敘述錯誤的是

A. 霧和霾的分散劑相同
B. 霧霾中含有硝酸銨和硫酸銨
C. NH3是形成無機顆粒物的催化劑
D. 霧霾的形成與過度施用氮肥有關
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】下列有關電化學的敘述,正確的是( )
A. 裝置工作時兩極均有氣泡產生,工作一段時間后溶液的堿性增強
裝置工作時兩極均有氣泡產生,工作一段時間后溶液的堿性增強
B.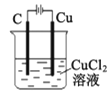 裝置工作一段時間后碳極上有紅色物質析出
裝置工作一段時間后碳極上有紅色物質析出
C.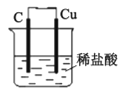 裝置可以模擬金屬的析氫腐蝕,銅棒一極的電極反應式為:2H++ 2e-=H2↑
裝置可以模擬金屬的析氫腐蝕,銅棒一極的電極反應式為:2H++ 2e-=H2↑
D.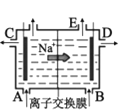 是陽離子交換膜法電解飽和食鹽水原理示意圖,E出口有黃綠色氣體放出
是陽離子交換膜法電解飽和食鹽水原理示意圖,E出口有黃綠色氣體放出
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】正丁醚是一種用途很廣的化工產品,毒性和危險性小,是安全性很高的有機溶劑,對許多天然及合成油脂、樹脂、橡膠、有機酸酯、生物堿等都有很強的溶解能力,還可作為電子級清洗劑和多種有機合成材料。可通過以下反應原理制取正丁醚:
2CH3CH2CH2CH2OH![]() CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
CH3CH2CH2CH2OCH2CH2CH2CH3+H2O
己知相關物質的部分信息如下:
沸點(℃) | 密度(g/cm3) | 溶解度(g) | 相對分子質量 | |
正丁醇 | 117.7 | 0.81 | 7.9 | 74 |
正丁醚 | 142 | 0.77 | 不溶于水 | 130 |
某課外化學學習小組查閱相關資料設計了以下實驗步驟合成正丁醚:
①在100 mL兩口燒瓶中加入30.0 mL正丁醇、5.0 mL濃硫酸和幾粒沸石,充分搖勻。在分水器中加入3.0 mL飽和食鹽水,按圖甲組裝儀器,接通冷凝水;
②反應:在電熱套上加熱,使瓶內液體微沸,回流反應約1小時。當餾液充滿分水器時,打開分水器放出一部分水。當水層不再變化,瓶中反應溫度達150 ℃,反應己基本完成,停止加熱;
③蒸餾:待反應液冷卻后,拆下分水器,將儀器改成蒸餾裝置如圖丙,再加幾粒沸石,蒸餾,收集餾分;
④精制:將餾出液倒入盛有10 mL水的分液漏斗中,充分振搖,靜置棄去水液,有機層依次用5 mL水,3 mL 5% NaOH溶液、3 mL水和3 mL飽和氯化鈣溶液洗滌,分去水層,將產物放入潔凈干燥的小錐形瓶中,然后加入0.2~0.4 9無水氯化鈣,再將液體轉入裝置丙中進行蒸餾,收集到餾分9.0 mL。
甲. 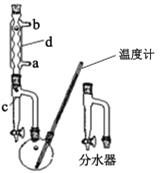 乙.
乙. ![]() 丙.
丙.
請根據以上操作回答下列問題:
(1)制備正丁醚的反應類型是___,儀器d的名稱是____。
(2)在步驟①中添加試劑的順序是____。相比裝置乙,裝置甲的優點是 ___。
(3)在步驟②中采用電熱套加熱而不采用酒精燈直接加熱的原因可能是____。
(4)在步驟③中收集餾分適宜的溫度范圍為____(填正確答案標號)。
A.115℃~ll9℃ B.140℃~144℃ C. 148℃~152℃
(5)在精制中,有機層在____層(填“上”或“下”),加入無水氯化鈣的作用是____。
(6)本小組實驗后所得正丁醚的產率約為 ___%(計算結果保留一位小數)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】過渡元素由于其特殊的核外電子排布而其有特殊的性質,成為化學研究的重點和前沿。
(l)過波元素處于周期表的____區和f 區。
(2)過渡元素能形成簡單化合物,還能形成多種配位化合物
① 通常,d軌道全空或全滿的過渡金屬離子與水分子形成的配合物無顏色,否則有顏色。如[Co(H2O)6]2+顯粉紅色,據此判斷,[Mn(H2O)6]2+____(填“有”或“無”)顏色。
② Ni2+可形成多種配合物,如Ni(CN)42-。寫出CN-的電子式____,若其中兩個CN-被NO2-替換,得到的配合物只有兩種結構,則Ni(CN)42-的空間構型是_____, NO2-的空間構型是_____,其中N原子的雜化方式是_____。
③ 從結構角度分析并比較CoF2與CoCl2晶體的熔點高低___________。
(3)金、銅等金屬及合金可用作生產石墨烯的催化劑,下圖是一種銅金合金的晶胞示意圖:

① 在該銅金合金的晶體中,與Cu原子距離相等且最近的Au原子數為_______。
② 原子坐標參數是用來表示晶胞內部各原子相對位置的指標,若A的原子坐標參數為(0,0,0);B的原子坐標參數為(0,1,0) , C的原子坐標參數為(l,0,0)。則D的原子子坐標參數為_________。
③ 若Au、Cu原子半徑分別為r1和r2,則該晶胞中的原子空間利用率為__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】化合物A經李比希法和質譜法分析得知其分子式為C8H8O2,相對分子質量為 136,A的核磁共振氫譜有4個峰且面積之比為1:2:2:3,A分子中只含一個苯環,且苯環上只有一個取代基,其核磁共振氫譜與紅外光譜如圖。關于A的下列說法中不正確的是( )
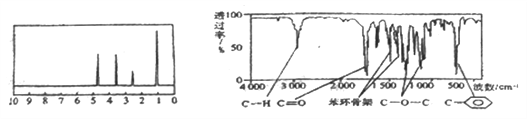
A. A分子屬于酯類化合物,在一定條件下能發生水解反應
B. A在一定條件下可與3 mol H2發生加成反應
C. 符合題中A分子結構特征的有機物只有一種
D. 與A屬于同類化合物的同分異構體只有2種
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com