
| A. | 在蒸餾水中滴加濃H2SO4,KW不變 | |
| B. | 向NaAlO2溶液中滴加NaHCO3溶液,有沉淀和氣體生成 | |
| C. | 中和等體積等物質(zhì)的量濃度的鹽酸和醋酸,所消耗的氫氧化鈉的物質(zhì)的量相同 | |
| D. | NaCl溶液和CH3COONH4溶液均顯中性,兩溶液中水的電離程度相同 |
分析 A、KW受溫度的影響;
B、NaHCO3溶液與NaAlO2溶液混合產(chǎn)生白色沉淀氫氧化鋁;
C、等體積等物質(zhì)的量濃度的鹽酸和醋酸的物質(zhì)的量相等;
D、CH3COONH4是弱酸弱堿鹽,在溶液中會水解,對水的電離有促進作用.
解答 解:A、KW只受溫度的影響,在蒸餾水中加入濃硫酸,由于濃硫酸稀釋放熱,故溫度升高,則Kw變大,故A錯誤;
B、NaHCO3溶液與NaAlO2溶液混合產(chǎn)生白色沉淀氫氧化鋁:HCO3-+AlO2-+H2O=A(OH)3↓+CO32-,無氣體放出,故B錯誤;
C、等體積等物質(zhì)的量濃度的鹽酸和醋酸的物質(zhì)的量相等,故消耗的氫氧化鈉的物質(zhì)的量相等,故C正確;
D、NaCl是強酸強堿鹽,在溶液中不水解,對水的電離無影響;CH3COONH4是弱酸弱堿鹽,在溶液中會水解,對水的電離有促進作用,兩溶液中水的電離程度不相同,故D錯誤.
故選C.
點評 本題考查了鹽類的水解、水的離子積的數(shù)值受溫度影響等問題,難度不大,應注意的是NaHCO3溶液與NaAlO2溶液混合產(chǎn)生白色沉淀氫氧化鋁的反應的書寫.


科目:高中化學 來源: 題型:填空題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題

 和
和 E、CH3CH2CH2CH3和
E、CH3CH2CH2CH3和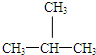
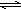 HCO3-+OH-
HCO3-+OH- 的系統(tǒng)命名為:3-甲基-4-乙基-庚烷
的系統(tǒng)命名為:3-甲基-4-乙基-庚烷 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 甲是一種可用于凈水和膨化食品的鹽,由A、B、C、D、E五種短周期元素組成.甲溶于水后可電離出三種離子,其中一種是由A、B形成的10電子陽離子.A元素原子核內(nèi)質(zhì)子數(shù)比E的少l,D、E同主族.某同學為探究甲的組成而進行如下實驗:
甲是一種可用于凈水和膨化食品的鹽,由A、B、C、D、E五種短周期元素組成.甲溶于水后可電離出三種離子,其中一種是由A、B形成的10電子陽離子.A元素原子核內(nèi)質(zhì)子數(shù)比E的少l,D、E同主族.某同學為探究甲的組成而進行如下實驗:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com