
 ;氯離子的電子式
;氯離子的電子式 .
.分析 (1)氯原子核外有17個電子,核外電子分為三個電子層;氯離子為陰離子,原子周圍有8個電子;
(2)氯氣與水反應生成HClO,HClO有漂白性;漂粉精的主要有效成分是次氯酸鈣;
(3)硫酸與氯化鈉反應生成HCl;
(4)氯氣用氫氧化鈉溶液吸收;根據元素的化合價變化判斷;
(5)氯氣是一種有著廣泛用途的重要化工原料.
解答 解:(1)氯原子是17號元素,核外電子分為三個電子層,一層2個電子,二層8個電子.三層7個電子,原子結構示意圖為 ;氯離子為陰離子,原子周圍有8個電子,氯離子的電子式為:
;氯離子為陰離子,原子周圍有8個電子,氯離子的電子式為: ;
;
故答案為: ;
; ;
;
(2)氯氣與水反應生成HClO,HClO有漂白性,則氯氣能使濕潤的有色布條褪色,起到漂白作用的物質是次氯酸;漂粉精的主要有效成分是次氯酸鈣,其化學式為Ca(ClO)2;
故答案為:次氯酸;Ca(ClO)2;
(3)實驗室制備氯化氫氣體利用原料氯化鈉和濃硫酸加熱反應生成氯化氫,微熱時生成硫酸氫鈉和氯化氫,反應的化學方程式為:NaCl+H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$NaHSO4+HCl↑,
故答案為:NaCl+H2SO4$\frac{\underline{\;\;△\;\;}}{\;}$NaHSO4+HCl↑;
(4)氯氣是有毒氣體,能與氫氧化鈉溶液反應,氯氣用氫氧化鈉溶液吸收;氯氣與NaOH反應時,Cl元素的化合價既升高又降低,所以氯氣既是氧化劑又是還原劑;
故答案為:NaOH溶液;c;
(5)氯氣是一種有著廣泛用途的重要化工原料,可用于制鹽酸、漂白粉、有機溶劑與多種農藥,
故答案為:制鹽酸;漂白粉.
點評 本題考查了氯元素單質以及化合物的性質,題目難度不大,題目涉及的知識點較多,側重于考查學生對基礎知識的綜合應用能力,注意把握氯氣的性質和用途.


 名師指導期末沖刺卷系列答案
名師指導期末沖刺卷系列答案 開心蛙口算題卡系列答案
開心蛙口算題卡系列答案科目:高中化學 來源:2016-2017學年江西省高二上第一次月考化學試卷(解析版) 題型:選擇題
少量鐵粉與100mL0.01mol/L的稀鹽酸反應,反應速率太慢。為了加快此反應速率而不改變H2的產量,可以使用如下方法中的( )
①加H2O ②加NaOH固體 ③滴入幾滴濃鹽酸 ④加CH3COONa固體⑤加NaCl溶液 ⑥滴入幾滴硫酸銅溶液 ⑦升高溫度(不考慮鹽酸揮發) ⑧改用10mL0.1mol/L鹽酸.
A.①⑥⑦ B.③⑤⑧ C.③⑦⑧ D.⑤⑦⑧
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 98g硫酸的摩爾數為1 mol | B. | 氧的摩爾質量為32g/mol | ||
| C. | 阿伏加德羅常數約為6.02×1023個 | D. | 某硫酸中H2SO4的質量分數為0.60 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | $\frac{V}{2}$L | B. | $\frac{V}{3}$L | C. | $\frac{5V}{6}$L | D. | VL |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
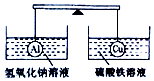 在杠桿的兩端分別掛著質量和體積都相同的空心鋁球和銅球,此時杠桿平衡.然后將兩球分別浸沒在氫氧化鈉溶液和硫酸鐵溶液中片刻,如圖,則下列說法正確的是( )
在杠桿的兩端分別掛著質量和體積都相同的空心鋁球和銅球,此時杠桿平衡.然后將兩球分別浸沒在氫氧化鈉溶液和硫酸鐵溶液中片刻,如圖,則下列說法正確的是( )| A. | 兩燒杯中均無氣泡產生 | B. | 左邊燒杯中的溶液質量增加了 | ||
| C. | 在浸沒過程中,杠桿始終保持平衡 | D. | 右邊銅球質量不變 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
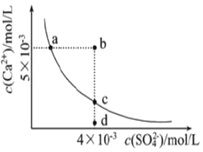
| A. | a、c兩點均可以表示常溫下CaSO4溶于水所形成的飽和溶液 | |
| B. | a點對應的Ksp不等于c點對應的Ksp | |
| C. | b點將有沉淀生成,平衡后溶液中c(Ca2+)•c(SO42-)一定等于9×10-6 | |
| D. | 向d點溶液中加入適量CaCl2固體可以變成c點 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
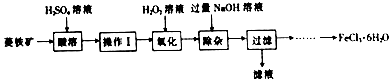
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com