
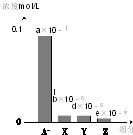
 常溫下,0.2mol/L的一元酸HA與等濃度的NaOH溶液等體積混合后,所得溶液中部分微粒組分及濃度如圖所示(a、b、d、e均為不超過1的正數),則下列說法正確的是( )
常溫下,0.2mol/L的一元酸HA與等濃度的NaOH溶液等體積混合后,所得溶液中部分微粒組分及濃度如圖所示(a、b、d、e均為不超過1的正數),則下列說法正確的是( )| A. | 該溶液pH=7 | B. | 該溶液中:c(A-)+c(Y)=c(Na+) | ||
| C. | HA為強酸 | D. | 圖中X表示HA,Y表示OH-,Z表示H+ |
分析 一元酸HA和NaOH溶液等體積、等濃度0.2mol/L混合,HA+NaOH=NaA+H2O,所得溶液中A-濃度小于0.1mol/L,說明在溶液中存在A-+H2O?HA+OH-,NaA水解,HA為弱酸,NaA溶液呈堿性,則c(OH-)>c(H+),一般來說,鹽類的水解程度較低,則有c(A-)>c(OH-),所以有:c(Na+)=0.1mol/L>c(A-)>c(OH-)>c(HA)>c(H+),即X表示OH-,Y表示HA,Z表示H+,溶液中存在物料守恒為:c(Na+)=c(A-)+c(HA).
A.該混合液pH>7;B.Y表示HA,溶液中存在物料守恒得到c(A-)+c(Y)=c(Na+);C.HA為弱酸;D.X表示OH-,Y表示HA,Z表示H+.
解答 解:一元酸HA和NaOH溶液等體積、等濃度0.2mol/L混合,HA+NaOH=NaA+H2O,所得溶液中A-濃度小于0.1mol/L,說明在溶液中存在A-+H2O?HA+OH-,NaA水解,HA為弱酸,NaA溶液呈堿性,則c(OH-)>c(H+),一般來說,鹽類的水解程度較低,則有c(A-)>c(OH-),所以有:c(Na+)=0.1mol/L>c(A-)>c(OH-)>c(HA)>c(H+),即X表示OH-,Y表示HA,Z表示H+,溶液中存在物料守恒得到:c(Na+)=c(A-)+c(HA).
A.所得溶液中A-濃度小于0.1mol/L,說明在溶液中存在A-+H2O?HA+OH-,NaA水解,c(Na+)>c(A-),由電荷守恒有:c(Na+)+c(H+)=c(A-)+c(OH-),該混合液pH>7,故A錯誤;
B.溶液中存在物料守恒c(Na+)=c(A-)+c(HA),Y表示HA,得到c(A-)+c(Y)=c(Na+),故B正確;
C.一元酸HA和NaOH溶液等體積、等濃度0.2mol/L混合,二者恰好反應:HA+NaOH=NaA+H2O,所得溶液為NaA溶液,溶液中中A-濃度小于0.1mol/L,說明在溶液中存在A-+H2O?HA+OH-,NaA水解,HA為弱酸,故C錯誤;
D.HA是弱電解質,則有c(A-)>c(OH-),c(OH-)除了水解產生的還有水電離的,因此c(OH-)>c(HA),所以有:c(Na+)=0.1mol/L>c(A-)>c(OH-)>c(HA)>c(H+),即X表示OH-,Y表示HA,Z表示H+,故D錯誤;
故選B.
點評 本題考查了酸堿混合溶液定性判斷,根據酸的強弱結合物料守恒、電荷守恒分析解答,考查離子濃度大小比較、溶液PH值、鹽類水解等,判斷一元酸HA是弱酸為解題關鍵,題目難度中等.


 提分百分百檢測卷單元期末測試卷系列答案
提分百分百檢測卷單元期末測試卷系列答案科目:高中化學 來源: 題型:選擇題
| A. | IA族,單質的熔點逐漸降低 | |
| B. | ⅥA族,對氣態氫化物還原性逐漸增強 | |
| C. | VA族氫化物的沸點逐漸升高 | |
| D. | ⅣA族最高氧化物對應水化物的酸性逐漸增強 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| pH | 2 | 4 | 6 | 6.5 | 8 | 13.5 | 14 |
| 腐蝕快慢 | 較快 | 慢 | abc 較快 | ||||
| 主要產物 | Fe2+ | Fe3O4 | Fe2O3 | FeO2- | |||
| A. | 當pH<4時,碳鋼主要發生析氫腐蝕 | |
| B. | 當pH>6時,碳鋼主要發生吸氧腐蝕 | |
| C. | 當pH>14時,正極反應為O2+4H++4e→2H2O | |
| D. | 在煮沸除氧氣后的堿性溶液中,碳鋼腐蝕速率會減緩 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
 室溫下,把SiO2細粉放入蒸餾水中,攪拌至平衡,生成H4SiO4溶液(SiO2+2H2O?H4SiO4),該反應平衡常數K隨溫度的變化如圖示,攪拌1小時,測得H4SiO4的質量分數為0.01%(溶液密度為1.0g/mL),下列分析正確的是( )
室溫下,把SiO2細粉放入蒸餾水中,攪拌至平衡,生成H4SiO4溶液(SiO2+2H2O?H4SiO4),該反應平衡常數K隨溫度的變化如圖示,攪拌1小時,測得H4SiO4的質量分數為0.01%(溶液密度為1.0g/mL),下列分析正確的是( )| A. | 該反應平衡常數的表達式為K=c(H4SiO4) | |
| B. | 該生成H4SiO4的反應為吸熱反應 | |
| C. | 用H4SiO4表示的反應速率為1.04×10-2mol/(L•h) | |
| D. | 若K值變大,在平衡移動時逆反應速率先減小后增大 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ${\;}_{62}^{144}$Sm與${\;}_{62}^{150}$Sm互為同素異形體 | |
| B. | ${\;}_{62}^{144}$Sm與${\;}_{62}^{150}$Sm具有相同核外電子排布 | |
| C. | ${\;}_{62}^{144}$Sm與${\;}_{62}^{150}$Sm的性質完全相同 | |
| D. | ${\;}_{62}^{144}$Sm與${\;}_{62}^{150}$Sm的質子數不同,但中子數相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
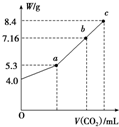 鈉有多種化合物,如氧化鈉、過氧化鈉、氫氧化鈉、碳酸鈉、碳酸氫鈉等等,這些物質在實際生活中有廣泛的應用,一定條件下相互間能進行轉化.完成下列計算:
鈉有多種化合物,如氧化鈉、過氧化鈉、氫氧化鈉、碳酸鈉、碳酸氫鈉等等,這些物質在實際生活中有廣泛的應用,一定條件下相互間能進行轉化.完成下列計算:查看答案和解析>>
科目:高中化學 來源: 題型:解答題
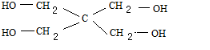 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,2.24LCCl4中含Cl原子數目為0.4NA | |
| B. | 白磷分子(P4)呈正四面體結構,12.4 g白磷中含有P-P鍵數目為0.6NA | |
| C. | 5.6 g鐵粉在2.24l(標準狀況)氯氣中充分燃燒,失去的電子數為0.3NA | |
| D. | 常溫常壓下,10 g46%酒精水溶液中含氧原子總數為0.1NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫常壓下,32g O2和16g O3的混合物中,含有O原子數目為2NA | |
| B. | 標準狀況下,1mol Na2O 和1mol Na2O2的混合物中,含有離子總數為7NA | |
| C. | 1mol NaHSO4溶于水或受熱熔化,電離出來的離子數目均為2NA | |
| D. | 在K35ClO3+6H37Cl=KCl+3Cl2↑+3H2O中,若生成71g Cl2,轉移的電子數目為 $\frac{2}{3}$NA |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com