
【題目】2020年5月1日北京市在全市范圍內開展施行垃圾分類,下列垃圾分類不正確是( )
A.魚骨、菜葉 | B.消毒劑及其包裝物 | C.破損的易拉罐 | D.破碎玻璃 |
|
|
|
|
廚余垃圾 | 有害垃圾 | 可回收垃圾 | 其他垃圾 |
A.AB.BC.CD.D
科目:高中化學 來源: 題型:
【題目】苯環中不存在碳碳單鍵和碳碳雙鍵交替的結構,可以作為證據的事實是( )
①苯是無色易揮發的液體;
②苯不能使酸性高錳酸鉀溶液褪色;
③![]() 和
和 是同一種物質。
是同一種物質。
A. ①②③ B. ①和② C. ①和③ D. ②和③
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】一定溫度下,向容積為2 L的密閉容器中通入兩種氣體發生化學反應,反應中各物質的物質的量變化如圖所示,對該反應的推斷合理的是( )
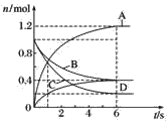
A.該反應的化學方程式為3B+4D![]() 6A+2C
6A+2C
B.反應進行到1 s時,v(A)=v(D)
C.反應進行到6 s時,B的平均反應速率為0.05 mol·L-1·s-1
D.反應進行到6 s時,各物質的反應速率相等
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氫氧化鋰(LiOH)是重要的初加T鋰產品之一,可用于繼續生產氟化鋰、錳酸鋰等,用天然鋰輝石(主要成分LiAISi2O3,含有Fe (III)等雜質)生產LiOH的一種工藝流程如圖所示:
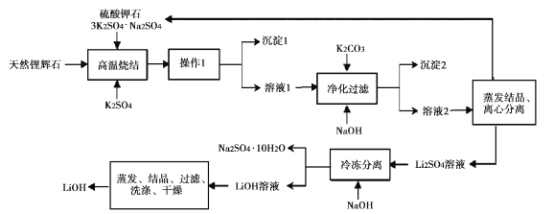
已知溶液1中含有Li+、K+、A13+、Na+、Fe3+、SO42-等離子,請回答相關問題。
(l)將LiAlSi2O6改寫為氧化物的形式:____。
(2)高溫燒結的目的是____。操作1是 __ 。
(3)凈化過濾過程中溶液的pH不能過低也不能過高,原因是____。
(4)流程中的某種物質可循環利用,該物質的化學式是____。
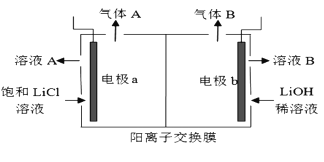
(5)工業生產中通過電解LiCI溶液的方法也可制得LiOH,其原理如圖所示,電極a應連接電源的____(選填“正極”或“負極”),電極b發生的反應是 ___,陽離子交換膜的作用是___
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】“點擊化學”是指快速、高效連接分子的一類反應,例如銅催化的Huisgen環加成反應:

我國科研人員利用該反應設計、合成了具有特殊結構的聚合物F并研究其水解反應。合成線路如下圖所示:
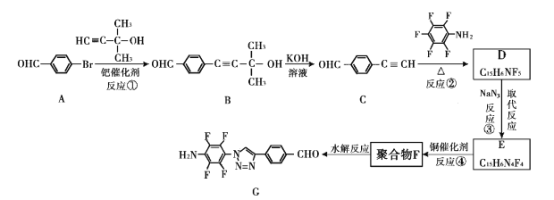
已知:![]()
(1)A生成B的反應類型是____。
(2)關于B和C,下列說法正確的是____(填字母序號)。
a 利用核磁共振氫譜可以鑒別B和C b B不能發生消去反應 c 可用酸性高錳酸鉀溶液檢驗C中含醛基
(3)B生成C的過程中還有另一種生成物X,分子式為C3H6O,核磁共振氫譜顯示只有一組峰,X的結構簡式為 ___。
(4)反應②的化學方程式為 ___。
(5)請根據以上流程,并推測聚合物F所具有的特殊結構,下列關于聚合物F的結構說法正確的是___
A F中必含 -CH2=N- 結構
B F中必含 -N=N- 結構
C F的結構可能是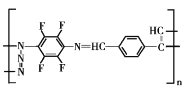
(6)H是比A多一個碳原子的同系物。H的同分異構體中符合下列條件的有 ___種。
①苯環上有三個取代基 ②能和FeCl3發生顯色反應
(7)為了探究連接基團對聚合反應的影響,設計了單體K,其合成路線如下,寫出H、I、J的結構簡式:___
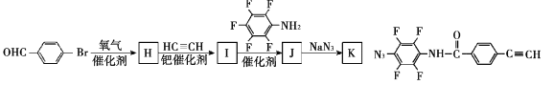
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】現有反應:mA(g)+nB(g)![]() pC(g),達到平衡后,當升高溫度時,B的轉化率變大;當減小壓強時,混合體系中C的質量分數減小,則:
pC(g),達到平衡后,當升高溫度時,B的轉化率變大;當減小壓強時,混合體系中C的質量分數減小,則:
(1)該反應的逆反應為________反應(填“吸熱”或“放熱”),且m+n________p(填“>”、“=”或“<”)。
(2)減壓使容器體積增大時,A的質量分數__________。(填“增大”、“減小”或“不變”,下同)
(3)若加入B(維持體積不變),則A的轉化率____________。
(4)若升高溫度,則平衡時B、C的濃度之比將____________。
(5)若加入催化劑,平衡時氣體混合物的總物質的量__________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】在1 L的密閉容器中,發生反應4A(s)+3B(g)![]() 2C(g)+D(g),經2 min后B的濃度減少0.6 mol·L-1。對此反應速率的正確表示是( )
2C(g)+D(g),經2 min后B的濃度減少0.6 mol·L-1。對此反應速率的正確表示是( )
A. 用A表示的反應速率是0.4 mol·L-1·min-1
B. 用BCD分別表示反應的速率,其比值是3∶2∶1
C. 在第2 min末的反應速率用B表示是0.3 mol·L-1·min-1
D. 在這2 min內用B表示的速率的值逐漸減小,用C表示的速率的值逐漸增大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】測定0.1mol·L-1Na2SO3溶液先升溫再降溫過程中的pH,數據如下表。實驗過程中,取①、④時刻的溶液,加入鹽酸酸化的BaCl2溶液做對比實驗,④產生白色沉淀多。下列說法不正確的是( )
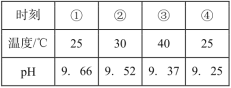
A.Na2SO3溶液中存在水解平衡:SO32-+H2O![]() HSO3-+OH-
HSO3-+OH-
B.④產生的白色沉淀是BaSO4
C.①→③的過程中,c(SO32-)在降低
D.①→③的過程中,溫度與c(SO32-)相比,前者對水解平衡的影響更大
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某研究性學習小組利用H2C2O4溶液和酸性KMnO4溶液的反應探究“外界條件的改變對化學反應速率的影響”,進行了如下實驗:
實驗序號 | 實驗 溫度/K | 有關物質 | 溶液顏色褪至無色所需時間/s | ||||
酸性KMnO4溶液 | H2C2O4溶液 | H2O | |||||
V/mL | c/mol·L-1 | V/mL | c/mol·L-1 | V/mL | |||
A | 293 | 2 | 0.02 | 4 | 0.1 | 0 | t1 |
B | T1 | 2 | 0.02 | 3 | 0.1 | V1 | 8 |
C | 313 | 2 | 0.02 | V2 | 0.1 | 1 | t2 |
(1)通過實驗A、B,可探究出___(填外部因素)的改變對化學反應速率的影響,其中V1=____、T1=____;通過實驗___(填實驗序號)可探究出溫度變化對化學反應速率的影響,其中V2=____。
(2)若t1<8,則由此實驗可以得出的結論是_____;忽略溶液體積的變化,利用實驗B中數據計算,0~8s內,用KMnO4的濃度變化表示的反應速率v(KMnO4)=___。
(3)該小組的一位同學通過查閱資料發現,上述實驗過程中n(Mn2+)隨時間的變化情況如圖所示,并認為造成這種變化的原因是反應體系中的某種粒子對KMnO4與草酸之間的反應有某種特殊作用,則該作用是____,相應的粒子最可能是___(填粒子符號)。
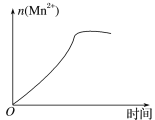
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com