
【題目】實驗室制備乙酸乙酯的實驗裝置如圖所示:
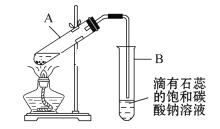
(1)A中濃硫酸的作用是________。
(2)實驗時預計試管B中產生的現象有:___、___(答2點)。
(3)欲從試管B中分離出乙酸乙酯,采用的方法是_______(填操作名稱);若要對產品乙酸乙酯進行干燥,__(填“能”或“不能”)用堿石灰干燥,理由是______。
(4)寫出實驗室用乙醇和乙酸制取乙酸乙酯的化學方程式:_______。
(5)若在A中加入4.6 g的乙醇、9.0 g的乙酸、數滴濃硫酸,緩慢加熱A至充分反應,最后將產品進行純化,得乙酸乙酯5.28 g,本實驗的產率是________。備注:產率指的是某種生成物的實際產量與理論產量的比值。
【答案】作催化劑和吸水劑,吸收水有利于平衡正向移動,產率更高; 有油狀液體生成 上層石蕊變為淺紅色 分液 不能 乙酸乙酯是酯,與堿石灰發生反應 CH3COOH + CH3CH2OH![]() CH3COOCH2CH3 + H2O 60%
CH3COOCH2CH3 + H2O 60%
【解析】
實驗室主要用無水乙酸和乙醇再濃硫酸加熱條件下反應生成乙酸乙酯,用飽和碳酸鈉溶液來接受乙酸乙酯,并分液得到乙酸乙酯,根據實驗用來理論計算出生成的乙酸乙酯的量,再根據實際產量計算產率。
⑴實驗室制備乙酸乙酯是在乙酸和乙醇濃硫酸加熱條件下反應,該反應是可逆反應,吸水有利于平衡正向移動,因此A中濃硫酸主要作用是催化劑和吸水劑,吸水有利于平衡正向移動,產率更高,故答案為:作催化劑和吸水劑,吸收水有利于平衡正向移動,產率更高;
⑵生成的乙酸乙酯進入到B中,乙酸乙酯不溶于飽和碳酸鈉溶液,再上層,油狀液體,還可能有未反應的乙酸和乙醇進入到B中,乙酸會使上層石蕊變淺紅色,因此實驗時預計試管B中產生的現象有:有油狀液體生成,上層石蕊變為淺紅色,故答案為:有油狀液體生成;上層石蕊變為淺紅色;
⑶乙酸乙酯不溶于碳酸鈉溶液,因此欲從試管B中分離出乙酸乙酯,采用的方法是分液,堿石灰是氧化鈣和氫氧化鈉的混合物,乙酸乙酯是酯,在堿性條件下要水解,因此不能用堿石灰干燥,理由是乙酸乙酯是酯,與堿石灰發生反應,故答案為:分液;不能;乙酸乙酯是酯,與堿石灰發生反應;
⑷實驗室用乙醇和乙酸制取乙酸乙酯的化學方程式CH3COOH + CH3CH2OH![]() CH3COOCH2CH3 + H2O,故答案為:CH3COOH + CH3CH2OH
CH3COOCH2CH3 + H2O,故答案為:CH3COOH + CH3CH2OH![]() CH3COOCH2CH3 + H2O;
CH3COOCH2CH3 + H2O;
⑸
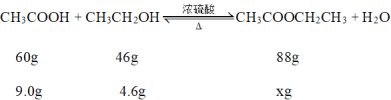
根據數據分析得出乙酸過量,只能按照乙醇進行計算,
![]()
解得x = 8.8g
![]() ,故答案為60%。
,故答案為60%。


 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化學 來源: 題型:
【題目】稱取4.00g氧化銅和氧化鐵固體混合物,加入50.0mL2.00mol·L-1的硫酸充分溶解,往所得溶液中加入5.60g鐵粉,充分反應后,得固體的質量為3.04g。請計算:
(1)加入鐵粉充分反應后,溶液中溶質的物質的量_________________。
(2)固體混合物中氧化銅的質量_________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】利用如圖所示裝置進行下列實驗,能得出相應實驗結論的是
選項 | ① | ② | ③ | 實驗結論 |
|
A | 濃鹽酸 | KMnO4 | NaOH | 能制取、收集氯氣并能吸收尾氣 | |
B | 濃氨水 | 生石灰 | 酚酞稀溶液 | 能制取氨氣并驗證氨氣的水溶液呈堿性 | |
C | 稀鹽酸 | Na2SO3 | Ba(NO3)2溶液 | SO2與可溶性鋇鹽均可生成白色沉淀 | |
D | 稀硫酸 | Na2CO3 | Na2SiO3溶液 | 非金屬性:S>C>Si |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】常溫下,NCl3是一種黃色黏稠狀液體,是制備新型水消毒劑ClO2的原料,可以采用如圖所示裝置制備NCl3。下列說法正確的是( )

A.每生成1 mol NCl3,理論上有4 mol H+經質子交換膜由右側向左側遷移
B.可用濕潤的KI-淀粉試紙檢驗氣體M
C.石墨極的電極反應式為NH4++3Cl--6e-===NCl3+4H+
D.電解過程中,電子的流動方向為電源負極→鉑棒→石墨棒→電源正極
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】利用下圖流程可制備1,4-環己二醇,試回答:
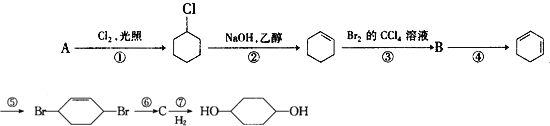
(1)反應①、②、③分別屬于___、____、___。(填反應類型)
(2)化合物![]() 中所含官能團的名稱為_______和________。
中所含官能團的名稱為_______和________。
(3)寫出下列化合物的結構簡式:A_________,C________。
(4)反應④所用的試劑和條件為_________________。
(5)寫出下列反應的化學方程式:反應①_____________;反應④_______________。
(6)請寫出以CH3CH2Br為原料制備HOCH2CH2OH的合成路線流程圖[無機試劑任用,合成路線流程圖示例見本題]。________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】用NA表示阿伏加德羅常數的值,下列判斷正確的是( )
A.標準狀況下,11.2 L H2O 中含有的氧原子數為0.5NA
B.5.6 g鐵與足量鹽酸反應轉移的電子數為0.3NA
C.16 g O2與16 g O3含有的氧原子數目相等
D.常溫常壓下,11.2 L氯氣所含原子數目為NA
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】室溫下,用滴定管量取一定體積的濃氯水置于錐形瓶中,用NaOH溶液以恒定速度來滴定該濃氯水,根據測定結果繪制出ClO-、ClO3-等離子的物質的量濃度c與時間t的關系曲線如下。下列說法正確的是( )
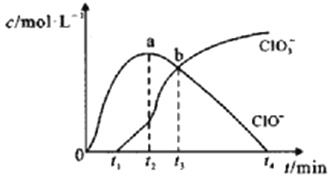
A.NaOH溶液和濃氯水可以使用同種滴定管盛裝
B.a點溶液中存在如下關系:c(Na+) + c(H+) = c(ClO-)+ c(OH-)+ c(ClO3-)
C.b點溶液中各離子濃度:c(Na+) > c(Cl-) > c(ClO-) = c(ClO3-)
D.t2~t4,ClO-的物質的量下降的原因可能是ClO-自身歧化:2ClO-= Cl-+ ClO3-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】對滴有酚酞試液的下列溶液,操作后顏色變深的是
A. 明礬溶液加熱 B. CH3COONa溶液加熱
C. 氨水中加入少量NH4Cl固體 D. 小蘇打溶液中加入少量NaCl固體
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com