
| A. | 向某無色溶液中加入BaCl2,產生白色渾濁說明該溶液中一定有SO42- | |
| B. | 向淀粉碘化鉀溶液中加氯水,溶液變為藍色說明氯氣的氧化性強于碘單質 | |
| C. | 某固體中加入稀鹽酸,產生了無色氣體,證明該固體一定有CO32- | |
| D. | 某溶液滴加稀鹽酸無明顯現象,再加硝酸銀產生白色沉淀,說明溶液中含Cl- |
分析 A.生成的沉淀可能為AgCl;
B.氯水中的氯氣氧化碘離子為碘單質,碘遇淀粉試液變藍色,氧化劑氧化性大于氧化產物;
C.該氣體為二氧化碳或二氧化硫,原溶液中可能含有碳酸氫根離子、亞硫酸根和亞硫酸氫根,不一定是碳酸根離子;
D.向某溶液中滴加稀鹽酸無明顯現象,再加硝酸銀產生白色沉淀,加入的鹽酸中含有氯離子,也會和銀離子反應生成白色沉淀.
解答 解:A.生成的沉淀可能為AgCl,應先加入鹽酸無沉淀,再加入BaCl2溶液產生白色沉淀,則試樣中一定有SO42-,故A錯誤;
B.向淀粉碘化鉀的溶液中加入氯水,溶液變為藍色,說明氯氣和碘離子發生置換反應生成碘,Cl2+2I-=I2+2Cl-,該反應中氯元素的化合價由0價變為-1價,碘元素的化合價由-1價變為0價,氯氣是氧化劑,碘是氧化產物,所以Cl2的氧化性強于I2,故B正確;
C.該氣體為二氧化碳或二氧化硫,原溶液中可能含有碳酸氫根離子、亞硫酸根和亞硫酸氫根,不一定是碳酸根離子,故C錯誤;
D.向某溶液中滴加稀鹽酸無明顯現象,再加硝酸銀產生白色沉淀,可能是加入的鹽酸中的氯離子生成的白色沉淀,不能說明原溶液中含Cl-,故D錯誤;
故選B.
點評 本題考查了離子檢驗的試劑選擇和實驗設計,注意干擾離子的分析判斷,離子性質和離子反應現象是解題關鍵,題目難度中等.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
| A. | 在多電子的原子里,能量高的電子通常在離核近的區域活動 | |
| B. | 核外電子總是先排在能量低的電子層上 | |
| C. | 兩種微粒,若核外電子排布完全相同,則其化學性質一定相同 | |
| D. | 微粒的最外層只能是8個或2個電子才穩定 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 含鈣、鋇、鉑等金屬的物質有絢麗的顏色,可用于制造焰火 | |
| B. | NO可用于某些疾病的治療 | |
| C. | 鹽堿地(含較多的NaCl、Na2CO3等)中施加適量石膏可降低土壤的堿性 | |
| D. | 雨后彩虹既是一種自然現象,又是一種光學現象,同時也與膠體有關 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,22.4L H2 與O2的混合氣體所含原子數為2NA | |
| B. | 標準狀況下,18g H2O的體積是22.4L | |
| C. | NA個SO2的體積是22.4L | |
| D. | 在常溫、常壓下,11.2L N2含有的分子數為0.5NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
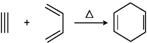 .若要合成
.若要合成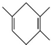 ,則所用的反應物可以是
,則所用的反應物可以是| A. | ①④ | B. | ①② | C. | ②④ | D. | ②③ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向NaOH溶液中逐滴滴入飽和氯化鐵溶液來制備Fe(OH)3膠體 | |
| B. | 向Fe(OH)3膠體中逐滴滴入稀鹽酸,現象是先出現紅褐色沉淀,后溶解轉為黃色溶液 | |
| C. | “丁達爾”效應是區分膠體和溶液的唯一手段 | |
| D. | 靜電除塵與膠體性質無關 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 依據圖甲可判斷正反應為放熱反應 | |
| B. | 在圖乙中,虛線可表示使用了催化劑 | |
| C. | 若正反應的△H<0,圖丙可表示升高溫度使平衡向逆反應方向移動 | |
| D. | 由圖丁中氣體平均相對分子質量隨溫度的變化情況,可推知正反應的△H>0 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
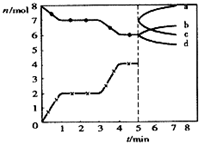 在體積為2L的密閉容器中進行下列反應:C(s)+CO2(g)═2CO(g);△H=+Q kJ•mol-1.如圖為CO2、CO的物質的量隨時間t的變化關系圖.下列說法不正確的是( )
在體積為2L的密閉容器中進行下列反應:C(s)+CO2(g)═2CO(g);△H=+Q kJ•mol-1.如圖為CO2、CO的物質的量隨時間t的變化關系圖.下列說法不正確的是( )| A. | 在0-1min內CO的物質的量增加了2mol | |
| B. | 當固焦炭的質量不發生變化時,說明反應已達平衡狀態 | |
| C. | 5min時再充入一定量的CO,n(CO)、n(CO2)的變化可分別由c、b曲線表示 | |
| D. | 3min時溫度由T1升高到T2,重新平衡時K(T2)小于K(T1) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com