
| A. | ④>①=②>③ | B. | ①>④>②>③ | C. | ④>①>③>② | D. | ④>②>①>③ |
分析 假設溶液體積為1L,分別計算溶液中溶質的物質的量,然后依據強電解質完全電離,弱電解質部分電離,弱堿陽離子、弱酸根離子部分水解的性質判斷解答.
解答 解:假設溶液體積為1L,濃度均為0.5mol•L-1相同體積的下列四種溶液,
含有KCl 物質的量為0.5mol,氯化鉀為強電解質,完全電離所以含有鉀離子物質的量為0.5mol;
含有FeCl3物質的量為0.5mol,氯化鐵為強電解質完全電離產生0.5mol三價鐵離子,鐵離子為弱堿陽離子,部分水解,所以溶液中三價鐵離子水解:Fe3++3OH-?Fe(OH)3+3H+,所以陽離子物質的量大于0.5mol;
含有HF物質的量為0.5mol,HF為弱電解質,部分電離,所以含有的氫離子小于0.5mol;
含有碳酸鈉的物質的量為0.5mol,碳酸鈉為強電解質完全電離,產生1mol鈉離子,所以含有陽離子物質的量為1mol;
所以:上述溶液中含有陽離子數目由多到少的順序為:④>②>①>③;
故選:D.
點評 本題考查了離子濃度大小比較,明確電解質強弱及電離方式,熟悉鹽類水解規律是解題關鍵,題目難度不大.


 閱讀快車系列答案
閱讀快車系列答案科目:高中化學 來源: 題型:選擇題
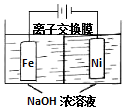 具有廣泛用途的Na2FeO4可用電解法制取:Fe+2H2O+2OH-$\frac{\underline{\;通電\;}}{\;}$FeO42-+3H2↑,其工作原理如圖所示.下列敘述正確的是( )
具有廣泛用途的Na2FeO4可用電解法制取:Fe+2H2O+2OH-$\frac{\underline{\;通電\;}}{\;}$FeO42-+3H2↑,其工作原理如圖所示.下列敘述正確的是( )| A. | 電解一段時間后,陽極室的c(OH-)增大 | |
| B. | Na+由陰極室移向陽極室 | |
| C. | 陰極反應式:2H2O+2e-=H2↑+2OH- | |
| D. | 電解過程中,當消耗1 mol OH-時,同時生成33.6 L H2 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
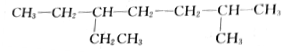 的名稱是2-甲基-5-乙基庚烷
的名稱是2-甲基-5-乙基庚烷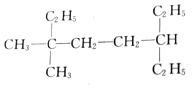 的名稱是3,3-二甲基-6-乙基辛烷
的名稱是3,3-二甲基-6-乙基辛烷 的名稱是2-甲基-3,6-二乙基辛烷
的名稱是2-甲基-3,6-二乙基辛烷 的名稱是2,4,4,5-四甲基庚烷.
的名稱是2,4,4,5-四甲基庚烷.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 現象 | 解釋或結論 | |
| A | 無色試劑瓶中的濃硝酸呈現黃色 | 硝酸不穩定,分解生成NO2的溶解在其中 |
| B | 在玻璃導管口點燃氫氣,火焰呈黃色 | 氫氣燃燒 |
| C | 某無色溶液中滴加氯水和四氯化碳,振蕩、靜置,下層出現紫色 | 溶液中含有碘離子 |
| D | 向CuSO4溶液中通入H2S,有黑色沉淀生成 | 有難溶的CuS生成 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
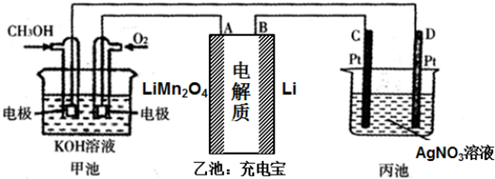
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
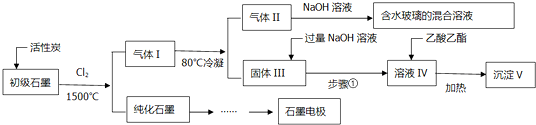
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 等濃度CH3COOH溶液與NH3•H2O溶液等體積混合后,存在c(NH4+)+c(H+)=c(CH3COO-)+c(OH-) | |
| B. | 等濃度的HCl溶液與CH3COOH溶液中c(H+)也相同 | |
| C. | 向20mLHCl溶液中加入10mL同一濃度的HCl溶液時,其pH會改變 | |
| D. | 等濃度的CH3COOH溶液和NaOH溶液等體積混合后,溶液顯中性 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
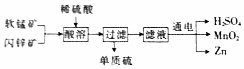 工業上可用軟錳礦(主要成分MnO2)和閃鋅礦(主要成分為ZnS)制備干電池中所需的MnO2和Zn,其工藝流程如圖所示,下列說法中錯誤的是( )
工業上可用軟錳礦(主要成分MnO2)和閃鋅礦(主要成分為ZnS)制備干電池中所需的MnO2和Zn,其工藝流程如圖所示,下列說法中錯誤的是( )| A. | 上述流程中錳元素的價態沒有變化 | |
| B. | 上述流程中的硫酸可循環利用 | |
| C. | 通電過程中,生成Zn單質時發生還原反應 | |
| D. | 通電過程中,陽極的電極反應式為Mn2+-2e-+2H2O═MnO2+4H+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | A、C的氧化物均含離子鍵 | |
| B. | C離子的半徑小于D離子的半徑 | |
| C. | A、B可形成多種原子個數比為1:1的化合物 | |
| D. | 含D元素的鹽溶液只能顯堿性 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com