
分析 (1)根據配制一定物質的量濃度的溶液方法驟排序;
(2)根據m=nM=cVM及天平的讀數情況計算氯化鈉的質量;
(3)如果加水超過了刻度線,需要重新配制;
(4)根據c=$\frac{n}{V}$分析操作對溶質的物質的量或對溶液的體積的影響判斷.
解答 解:(1)配制一定物質的量濃度的溶液的步驟有:計算、稱量、溶解、冷卻、移液、洗滌、定容、搖勻等操作,所以正確的操作順序為:①②④③⑤,
故答案為:①②④③⑤;
(2)需要氯化鈉的質量為:m=nM=cVM=0.5mol•L-1×0.5L×58.5g/mol=14.625g,天平的最小讀數為0.1g,則需要稱量的NaCl的質量為:14.6g,
故答案為:14.6g;
(3)定容時,如果加水超過了刻度線,溶液的體積偏大,導致配制溶液的濃度偏低,此次配制失敗,需要重新配制,
故答案為:需重新配制溶液;
(4)①定容時,俯視刻度線,導致溶液的體積偏小,所以配制溶液的濃度偏高,
故答案為:偏高;
②移液后,未洗滌燒杯和玻璃棒,導致溶質的物質的量偏小.所以配制溶液的濃度偏低,
故答案為:偏低.
點評 本題考查了一定物質的量濃度溶液的配制,題目難度不大,注意掌握配制一定物質的量濃度的溶液方法,易錯題是(4)題,誤差的分析是學習的難點,會根據c=$\frac{n}{V}$分析操作對溶質的物質的量或對溶液的體積的影響來判斷配制溶液的濃度是偏高還是偏低.


 名校課堂系列答案
名校課堂系列答案科目:高中化學 來源: 題型:解答題
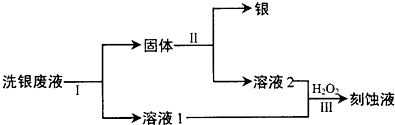
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
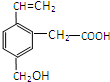 某有機物的結構如圖所示,這種有機物不可能具有的性質是
某有機物的結構如圖所示,這種有機物不可能具有的性質是| A. | ①④ | B. | 只有⑥ | C. | 只有③ | D. | ④⑥ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 相同 | B. | 中和HCl的多 | C. | 中和CH3COOH的多 | D. | 無法比較 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 (1)18電子分子中含有4個原子,其結構式是H-O-O-H或PH3
(1)18電子分子中含有4個原子,其結構式是H-O-O-H或PH3查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | CH2=CH2 | B. | CH≡C-CH3 | C. | CH2=CH2 | D. | CH2=CH-CH=CH2 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1mol Na2O2固體中含有的陰離子數為2NA | |
| B. | 常溫常壓下,3.2g CH4中含有的電子數為2NA | |
| C. | 標準狀況下,11.2L乙酸乙酯中含有的分子數為0.5NA | |
| D. | 100mL 1mol•L-1 CH3COOH溶液中含有的CH3COOH分子數為0.1NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | 0-6min的平均反應速率:v(H2O2)≈3.3×10-2mol/(L•min) | |
| B. | 6-10min的平均反應速率:v(H2O2)<3.3×10-2mol/(L•min) | |
| C. | 反應到6min時,H2O2分解了50% | |
| D. | 反應到6min時,c(H2O2)=0.30mol/L |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 3.6g重水中含有的中子數為2NA | |
| B. | 16.0g的過氧(根)離子中含有的電子數為9NA | |
| C. | 100mL 3.0mol/L的鹽酸與5.6g鐵屑完全反應轉移的電子數為0.3NA | |
| D. | 含2mol H2SO4的濃硫酸與足量金屬銅完全反應,產生SO2分子數為NA |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com