
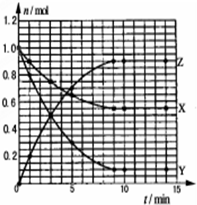
 某溫度時,在2L密閉容器中氣態物質X和Y反應生成氣態物質Z,它們的物質的量隨時間的變化如圖所示,則下列說法錯誤的是( )
某溫度時,在2L密閉容器中氣態物質X和Y反應生成氣態物質Z,它們的物質的量隨時間的變化如圖所示,則下列說法錯誤的是( )| A. | 反應的化學方程式是X+2Y?2Z | |
| B. | 該反應在0-3min時間內產物Z的平均反應速率0.083mol•L-1•min-1 | |
| C. | 由圖象知該反應吸收能量 | |
| D. | 其他條件不變,升高溫度,若正反應速率增大,則逆反應速率將減小 |
分析 A、依據圖象計算達到平衡狀態各物質的物質的量變化,物質的量變化之比等于化學方程式計量數之比,據此寫出化學方程式;
B、反應速率V=$\frac{△c}{△t}$計算得到;
C、圖象是物質在反應過程中物質的量的變化曲線,不能判斷反應熱量變化;
D、升高溫度增大反應速率,正逆反應速率都增大.
解答 解:A、依據圖象計算達到平衡狀態各物質的物質的量變化,物質的量變化之比等于化學方程式計量數之比,物質的量變化分析XY為反應物,Z為生成物,物質的量變化之比為,n(X):n(Y):n(Z)=(1.0mol-0.55mol):(1.0mol-0.1mol):0.9mol=1:2:2,據此寫出化學方程式為X+2Y?2Z,故A正確;
B、反應速率V=$\frac{△c}{△t}$,該反應在0-3min時間內產物Z的平均反應速率=$\frac{\frac{0.5mol}{2L}}{3min}$=0.083mol•L-1•min-1,故B正確;
C、圖象只是反應物和生成物物質的量變化趨勢,不能表達反應隨溫度的變化,故C錯誤;
D、升高溫度增大反應速率,正逆反應速率都增大,只是增大程度不同,故D錯誤;
故選CD.
點評 本題考查了化學圖象的分析判斷,化學反應速率、轉化率概念的計算分析,主要是化學方程式書寫方法和影響反應速率因素的理解應用,掌握基礎是關鍵,題目較簡單.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小學生10分鐘應用題系列答案
小學生10分鐘應用題系列答案科目:高中化學 來源: 題型:選擇題
| A. | 含0.1 mol/L-1SO2的溶液中:Na+、Ba2+、Br-、Cl- | |
| B. | 能與金屬鋁反應放出氫氣的溶液中:K+、Mg2+、NO3-、SO42- | |
| C. | 堿性溶液中:K+、NH4+、SO42-、NO3- | |
| D. | 不能使酚酞變紅的無色溶液中:Na+、K+、MnO4-、I- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | X的最高價氧化物對應的水化物是弱酸 | |
| B. | 元素Z位于元素周期表的第3周期Ⅵ族 | |
| C. | Y形成的單質能在二氧化碳中燃燒 | |
| D. | 原子半徑的大小順序:r(Z)>r(Y)>r(X) |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 溶液中c(B-)為1.6×10-3mol/L | |
| B. | 溶液中c(B-)為1.7×10-13mol/L | |
| C. | AB2比AC更難溶解 | |
| D. | 因兩者不同類而無法比較其溶解度的大小 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 用銅電極電解飽和氯化鈉溶液:2Cl-+2H2O$\frac{\underline{\;電解\;}}{\;}$2OH-+H2↑+Cl2↑ | |
| B. | 過量鐵與氯氣反應:2Fe+3Cl2$\frac{\underline{\;\;△\;\;}}{\;}$2FeCl3 | |
| C. | 過氧化鈉與水反應:2O22-+2H2O=4OH-+O2↑ | |
| D. | 向石灰水中滴加少量Ca(HCO3)2溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 石墨轉化為金剛石不是化學變化 | |
| B. | 金剛石比石墨穩定 | |
| C. | 1mol石墨具有的總能量比1mol金剛石的低 | |
| D. | 等質量的石墨與金剛石完全燃燒,石墨放出的能量多 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
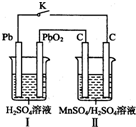 錳及其化合物應用越來越廣泛,MnO2是一種重要的無機功能材料,制備MnO2的方法之一是以石墨為電極,電解酸化的MnSO4溶液,陽極的電極反應式為Mn2+-2e-+2H20=MnO2+4H+.
錳及其化合物應用越來越廣泛,MnO2是一種重要的無機功能材料,制備MnO2的方法之一是以石墨為電極,電解酸化的MnSO4溶液,陽極的電極反應式為Mn2+-2e-+2H20=MnO2+4H+.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
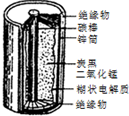 某學校設計了一節實驗活動課,讓學生從廢舊的鋅錳酸性干電池中回收碳棒、MnO2、NH4Cl、ZnCl2等物質,整個實驗過程如下,請回答有關問題:
某學校設計了一節實驗活動課,讓學生從廢舊的鋅錳酸性干電池中回收碳棒、MnO2、NH4Cl、ZnCl2等物質,整個實驗過程如下,請回答有關問題:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com