
分析 (1)根據配制步驟是計算、稱量、溶解、冷卻、移液、洗滌、定容、搖勻、裝瓶來分析需要的儀器;
(2)根據使用玻璃棒的操作來分析其用途;
(3)溶解、轉移溶液后未對燒杯和玻璃棒進行洗滌,會導溶質的損失;
(4)溶液為均一穩定分散系,取出任意體積都和原溶液濃度相等;根據m=CVM來計算;
根據溶液稀釋前后溶質的物質的量不變計算稀釋后溶質的物質的量濃度.
解答 解:(1)根據配制步驟是計算、稱量、溶解、冷卻、移液、洗滌、定容、搖勻、裝瓶可知所需的儀器:托盤天平、燒杯、玻璃棒、500mL容量瓶、膠頭滴管.
故還缺少的儀器是膠頭滴管,故答案為:膠頭滴管;
(2)在配制過程中,溶解氫氧化鈉固體時玻璃棒的用途是:攪拌,加速溶解;在移液時玻璃棒的用途是引流,
故答案為:攪拌、加速溶解;引流;
(3)溶解、轉移溶液后未對燒杯和玻璃棒進行洗滌,會導溶質的損失,則溶液濃度偏小,故答案為:偏小;
(4)溶液為均一穩定分散系,取出任意體積都和原溶液濃度相等,從中取出10mL,其物質的量濃度為1.0mol/L;
根據m=CVM可知,含有的氫氧化鈉的質量m=1.0mol/L×0.01L×40g/mol=0.4g.
溶液稀釋前后溶質的物質的量不變,這10mL溶液用水稀釋到100mL,所得溶液中溶質的物質的量濃度為$\frac{0.01L×1.0mol/L}{0.1L}$=0.1mol/L;
故答案為:1;0.4;0.1.
點評 本題考查物質的量濃度計算,題目難度不大,注意有關計算公式的運用,把握溶液的特點以及溶液稀釋前后溶質的物質的量不變的特征.


 名師指導期末沖刺卷系列答案
名師指導期末沖刺卷系列答案 開心蛙口算題卡系列答案
開心蛙口算題卡系列答案科目:高中化學 來源: 題型:選擇題
| A. | 水晶有固定的熔點,而普通玻璃則沒有 | |
| B. | 水泥、玻璃、陶瓷屬于傳統的無機非金屬材料 | |
| C. | 不銹鋼和普通鋼的組成元素完全相同,但耐腐蝕性能不同 | |
| D. | 氯化銨和單質碘在加熱時有類似現象,但本質不同 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題

| A. | N2O4(g)?2NO2(g) | B. | CO2(g)+C(s)?2CO(g) | ||
| C. | 2SO2(g)+O2(g)?2SO3(g) | D. | 4NH3(g)+5O2(g)?4NO(g)+6H2O(g) |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
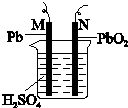 已知鉛蓄電池的反應原理是:Pb(s)+PbO2(s)+2H2SO4(aq)═2PbSO4(s)+2H2O(l)△H<0圖為鉛蓄電池的示意圖.下列說法正確的是( )
已知鉛蓄電池的反應原理是:Pb(s)+PbO2(s)+2H2SO4(aq)═2PbSO4(s)+2H2O(l)△H<0圖為鉛蓄電池的示意圖.下列說法正確的是( )| A. | 充電時,陽極的電極反應式為:PbSO4+2e-═Pb+SO42- | |
| B. | 充電時,若N連接電源正極,則該極生成PbO2 | |
| C. | 放電時,c(H2SO4)不變,兩極的質量增加 | |
| D. | 放電時,N為負極,其電極反應式為:PbO2+SO42-+4H++2e-═PbSO4+2H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 實驗步驟 | 實驗現象 | 實驗結論 |
Ⅰ.取第一份溶液和適量稀鹽酸加入下列裝置的試管中,把澄清的石灰水加入燒杯中 | 氣泡產生,澄 清的石灰水變渾濁 | 證明含有碳酸根離子 |
| Ⅱ.取第二份溶液,分別滴加稀鹽酸和氯化鋇 | 白色沉淀 | 證明含有硫酸根離子 |
| Ⅲ.取第三份溶液加入過量BaCl2溶液,過濾,除去SO42-和CO32-,再滴加AgNO3溶液和稀硝酸 | 有白色沉淀生成生成 | 證明含有氯離子 |
| Ⅳ.取第四份溶液進行焰色反應 | 透過藍色鈷玻璃 火焰呈紫色 | 證明含有K+ |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | pH=2與pH=1的硝酸中c(H+)之比為1:10 | |
| B. | 0.2mol/L與0.1mol/L醋酸中c(H+)之比為2:1 | |
| C. | pH相等NaOH與Ba(OH)2的溶液中c(OH-)之比為1:2 | |
| D. | 0.1mol/L醋酸與0.1mol/L醋酸鈉溶液中c(CH3COO-)之比為1:1 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 石蠟油(主要是含17個碳原子以上液態烷烴混合物)分解實驗按如圖所進行:
石蠟油(主要是含17個碳原子以上液態烷烴混合物)分解實驗按如圖所進行:查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com