
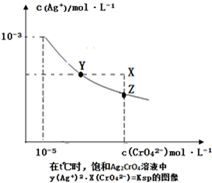
 已知t℃時AgCl的Ksp=4×10-l0,在t℃時,Ag2CrO4在水中的沉淀溶解平衡曲線如圖所示.下列說法錯誤的是( )
已知t℃時AgCl的Ksp=4×10-l0,在t℃時,Ag2CrO4在水中的沉淀溶解平衡曲線如圖所示.下列說法錯誤的是( )| A、在t℃時,Ag2CrO4的Ksp為1×10-11 |
| B、在飽和溶液中加入K2CrO4可使溶液由Y點到Z點 |
| C、在t℃時,Ag2CrO4(s)+2Cl-(aq)?2AgCl(s)+CrO42-(aq)平衡常數K=6.25×107 |
| D、在t℃時,以0.001mol/L AgNO3溶液滴定20mL 0.001mol/L KCl和0.001mol/L的K2CrO4的混和溶液,CrO42-先沉淀 |
| c(CrO42-) |
| c2(Cl-) |
| Ksp(Ag2CrO4) |
| Ksp2(AgCl) |
| 10-9 |
| (4×10-10)2 |
|
| 4×10-10 |
| 10-3 |


 世紀百通期末金卷系列答案
世紀百通期末金卷系列答案科目:高中化學 來源: 題型:
| A、赤鐵礦的主要成分是Fe3O4 |
| B、鐵與水蒸氣在高溫下的反應產物為Fe2O3和H2 |
| C、除去FeCl2溶液中的FeCl3雜質,向溶液中加入過量鐵粉,過濾 |
| D、FeCl3與KSCN產生紅色沉淀 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、NH4Cl |
| B、NaOH |
| C、MgSO4 |
| D、NaNO3 |
查看答案和解析>>
科目:高中化學 來源: 題型:
查看答案和解析>>
科目:高中化學 來源: 題型:
| 元素 | 有關性質或結構信息 |
| A | 負二價的A元素的氫化物在通常狀況下是一種液體,其中A的質量分數為88.9% |
| B | B原子得到一個電子后3p軌道全充滿 |
| C | C原子的p軌道半充滿,它的氣態氫化物能與其最高價氧化物的水化物反應生成一種常見的鹽X |
| D | D元素的最高化合價與最低化合價的代數和為零,其最高價氧化物為分子晶體 |
| E | E元素的核電荷數等于A原子核B元素氫化物的核電荷數之和 |
查看答案和解析>>
科目:高中化學 來源: 題型:
| A、加入催化劑有利于合成氨的反應 |
| B、對于反應2HI(g)?H2(g)+I2(g),增大平衡體系的壓強(壓縮體積),可使體系顏色變深 |
| C、500℃左右比室溫更有利于合成氨反應 |
| D、高壓條件有利于合成氨反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com