
如圖所示,其中甲池的總反應式為::2CH3OH+3O2+4KOH=2K2CO3+6H2O。下列說法正確的是
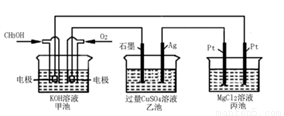
A. 甲池是電能轉化為化學能的裝置,乙、丙池是化學能轉化電能的裝置
B. 甲池通入CH3OH的電極反應為CH3OH-6e-+2H2O=CO32-+8H+
C. 反應一段時間后,向乙池中加入一定量Cu(OH)2固體,能使CuSO4溶液恢復到原濃度
D. 甲池中消耗280 mL(標準狀況下)O2,此時丙池中理論上最多產生1.45g固體
科目:高中化學 來源:2016-2017學年廣東省高二上學期期末考試化學(理)試卷(解析版) 題型:簡答題
冬季是霧霾天氣高發的季節,其中汽車尾氣和燃煤尾氣是造成霧霾的原因之一。
(1)汽車尾氣凈化的主要原理為:2NO(g)+2CO(g)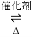 2CO2(g)+N2(g)
2CO2(g)+N2(g)
①在一定條件下,在一個容積固定為2L的密閉容器中充入0.8molNO和1.20molCO,開始反應至3min時測得CO的轉化率為20%,則用N2表示的平均反應速率為V(N2)=__________。
②對于氣相反應,用某組分(B)的平衡壓強(PB)代替物質的量濃度(CB)也可以表示平衡常數(記作Kp),則該反應平衡常數的表達式Kp=______________。
③該反應在低溫下能自發進行,該反應的△H_______0,(選填“>”、“=”或“<”)
④在某一絕熱,恒容的密閉容器中充入一定量的NO、CO發生上述反應,測得正反應的速率隨時間變化的曲線如圖所示(已知t2—t1=t3—t2)。則下列說法不正確的是__________。(填編號)
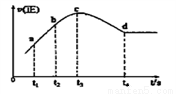
A.反應在c點未達到平衡狀態 B.反應速率a點小于b點
C.反應物濃度a點大于b點 D.NO的轉化率t1—t2=t2—t3
(2)使用甲醇汽油可能減少汽車尾氣對環境的污染,某化工廠用水煤氣為原料合成甲醇,恒溫條件下,在體積可變的密閉容器中發生反應:CO(g)+2H2(g)?CH3OH(g),到達平衡時,測得CO、H2、CH3OH分別為1mol、1mol、1mol,容器的體積為3L,現往容器中繼續通人3mol CO,此時v(正)____v(逆)(選填‘‘>”、“<’’或“=”),判斷的理由____________。
(3)二甲醚也是清潔能源,用合成氣在催化劑存在下制備二甲醚的反應原理為:
2CO(g)+4H2(g)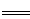 CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)
已知一定條件下,該反應中CO的平衡轉化率隨溫度、投料比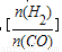 的變化曲線如圖:
的變化曲線如圖:
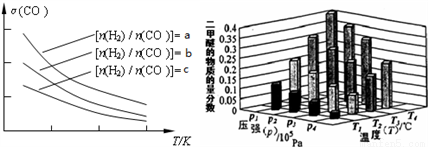
①a、b、c按從大到小的順序排序為___________。
②某溫度下,將2.0mol CO(g)和4.0mol H2(g)充入容積為2L的密閉容器中,反應到達平衡時,改變壓強和溫度,平衡體系中CH3OCH3(g)的物質的量分數變化情況如上圖所示,關于溫度和壓強的關系判斷正確的是___________;
A.P3>P2,T3>T2 B.P1>P3,T1>T3
C.P2>P4,T4>T2 D.P1>P4,T2>T3
③在恒容密閉容器里按體積比為1:2充入一氧化碳和氫氣,一定條件下反應達到平衡狀態.當改變反應的某一個條件后,下列變化能說明平衡一定向逆反應方向移動的是___________:
A.正反應速率先增大后減小
B.逆反應速率先增大后減小
C.化學平衡常數K值增大
D.反應物的體積百分含量增大
E.混合氣體的密度減小
F.氫氣的轉化率減小
查看答案和解析>>
科目:高中化學 來源:2016-2017學年湖北省宜昌市高二上學期期末考試化學試卷(解析版) 題型:選擇題
生產、生活離不開化學,下列說法不正確的是
A. 泡沫滅火器的反應原理是非氧化還原反應
B. 鋼鐵析氫腐蝕和吸氧腐蝕的速率一樣快
C. 鍋爐水垢中含有的CaSO4,可先用Na2CO3溶液處理,后用酸除去
D. 燃料電池的燃料都在負極發生反應
查看答案和解析>>
科目:高中化學 來源:2017屆河北省高三上學期期末考試理綜化學試卷(解析版) 題型:簡答題
甲、乙兩化學小組擬根據氨氣還原氧化銅反應的原理測定某銅粉樣品(混有CuO粉未)中金屬銅的含量。
(1)甲小組利用下圖裝置(可以重復選用),通過測定反應生成水的質量來達到實驗目的。
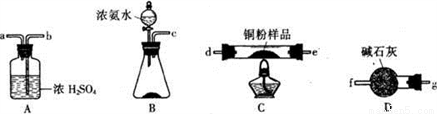
①按氣流方向連接各儀器接口,順序為______________(填小寫字母序號)。
②裝置B中固體試劑的名稱為____________________。
③裝置A的作用為____________。
④下列兩步操作應該先進行的是___________(填序號):i.加熱反應管 ii.向錐形瓶中逐滴滴加濃氨水,原因為________________________。
(2)乙小組利用上述裝置通過測定反應前后裝置C中固體的質量變化來達到實驗目的。
①按氣流方向連接各裝置,順序為______________(填大寫字母序號)。
②稱取m1 g銅粉樣品,測得反應前裝置C的質量為m2 g,充分反應后裝置C的質量為m3g。寫出樣品中金屬銅的質量分數表達式__________________。
(3)從稀鹽酸、濃硝酸、蒸餾水、雙氧水中選用合適的試劑,重新設計一個測定樣品中金屬銅含量的實驗方案(寫出主要步驟,不必描述操作過程的細節)_____________________________。
查看答案和解析>>
科目:高中化學 來源:2017屆河北省高三上學期期末考試理綜化學試卷(解析版) 題型:選擇題
化學與生產生活密切相關,下列物質的用途及解釋均正確的是
選項 | 用途 | 解釋 |
A | 可用FeCl3溶液刻蝕銅制電路板 | Fe3+的氧化性強于Cu2+ |
B | 碳與石英反應可冶煉粗硅 | 碳的非金屬性比硅強 |
C | 四氯化碳可用于滅火 | 四氯化碳的沸點高 |
D | 酸性KMnO4溶 液可漂白織物 | KMnO4有強氧化性 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源:2016-2017學年甘肅省天水市高二下學期開學考試(寒假作業檢測)化學試卷(解析版) 題型:選擇題
不能用勒夏特列原理解釋的是
①打開雪碧的瓶蓋,立即有氣體逸出
②由H2、I2、HI三種氣體組成的平衡體系加壓后顏色變深
③可用濃氨水和氫氧化鈉固體混合來快速制氨
④煅燒粉碎的硫鐵礦有利于SO2生成
⑤使用鐵觸媒,使N2和H2的混合氣體有利于合成NH3
⑥將混合氣體中的氨氣液化有利于合成氨反應
⑦500℃左右比室溫更有利于合成NH3
⑧配制FeCl2溶液時加入少量鐵屑
⑨實驗室常用排飽和和食鹽水法收集Cl2
A. 3項 B. 4項 C. 5項 D. 6項
查看答案和解析>>
科目:高中化學 來源:2016-2017學年甘肅省天水市高二下學期開學考試(寒假作業檢測)化學試卷(解析版) 題型:選擇題
銅鋅原電池(如圖)工作時,下列敘述正確的是( )
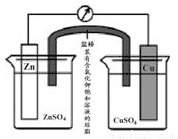
A. 在外電路中,電流從Zn極流向Cu極
B. 鹽橋中的Cl﹣移向CuSO4溶液
C. 當負極減小65g時,正極增加65g
D. 電池的總反應為 Zn+Cu2+=Zn2++Cu
查看答案和解析>>
科目:高中化學 來源:2016-2017學年江西省景德鎮市高二(素質班)上學期期末考試化學試卷(解析版) 題型:選擇題
已知丁基(—C4H9)有四種結構,某烴的結構簡式為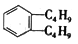 ,該烴可能的結構有( )
,該烴可能的結構有( )
A. 16種 B. 14種 C. 12種 D. 10種
查看答案和解析>>
科目:高中化學 來源:2017屆廣西省高三2月份模擬演練理綜化學試卷(解析版) 題型:選擇題
下列各組離子在指定溶液中,可能大量共存的是
A. 加入鋁能放出H2的溶液中:NH4+、Na+、Cl-、Br-
B. 水電離出的c(H+)=10-13mol·L-1的溶液中:Fe3+、K+、CO32-、SO32-
C. 室溫下, 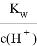 =0.1mol·L-1的溶液中:Al3+、Na+、SiO32-、HCO3-
=0.1mol·L-1的溶液中:Al3+、Na+、SiO32-、HCO3-
D. 使石蕊變紅的溶液中:Fe2+、K+、ClO-、SO42-
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com