
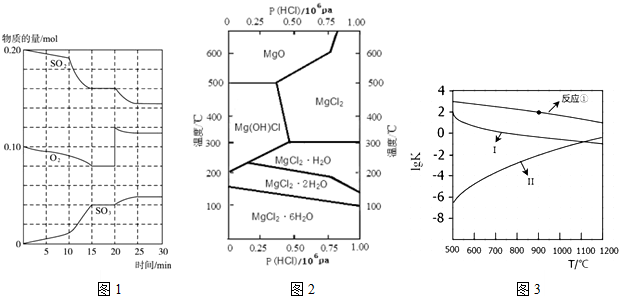
分析 (1)①由圖可知,反應進行至20min時,根據v=$\frac{△c}{△t}$計算;
②由圖可知,反應向正反應進行,10min到15min反應混合物單位時間內的變化量增大,說明反應速率增大,10min改變瞬間,各物質的物質的量不變;由圖可知,反應進行至20min時,改變體積,平衡向正反應移動,瞬間只有氧氣的濃度增大;
③當化學反應達到平衡狀態時,正逆反應速率相等,各物質的濃度不再發生變化,據此分析解答該題;
(2)A.由圖可知溫度低于100℃,MgCl2•6H2O不會發生分解;
B.由圖可知P(HCl)g=0.25MPa,溫度從300℃升高到500℃時MgCl2•6H2O晶體由Mg(OH)Cl轉變成MgO;
C.加熱MgCl2•6H2O晶體,P(HCl)g較小,鎂離子水解生成氫氧化鎂,得不到氯化鎂,若要得到無水氯化鎂,則應通入HCl,而增大P(HCl)g,抑制鎂離子的水解;
D.由圖可知在HCl氣體壓強為0.25×106Pa時,溫度由室溫升高至300℃,發生的反應為MgCl2•6H2O═Mg(OH)Cl+HCl+5H2O;
(3)根據反應①-③的平衡常數的對數lgK隨反應溫度T的變化曲線進行判斷變化規律.
解答 解:(1)①由圖可知,反應進行至20min時,SO3的物質的量變化為0.04mol,則反應平均速率為:v=$\frac{\frac{0.04mol}{2L}}{20}$=0.001mol•L-1•min-1,
故答案為:0.001mol•L-1•min-1;
②由圖可知,反應向正反應進行,10min到15min反應混合物單位時間內的變化量增大,說明反應速率增大,10min改變瞬間,各物質的物質的量不變,所以改變的條件即為增大反應速率,可選AE;
由圖可知,反應進行至20min時,平衡向正反應移動,瞬間只有氧氣的濃度增大,應是增大了氧氣的濃度,所以選C,
故答案為:AE;C;
③A.反應前后氣體的總質量一直不變,所以總質量不再變化不能說明達到了平衡狀態,故A錯誤;
B.SO2的轉化率達到最大,且保持不變,說明達到了平衡狀態,故B正確;
C.沒有指明正逆反應速率,不能說明達到了平衡狀態,故C錯誤;
D.反應物和生成物中氣體的計量數之和不等,容器中壓強不變,能證明達到了平衡狀態,故D正確;
故答案為:BD;
(2)A.由圖可知溫度低于100℃,MgCl2•6H2O不會發生分解,故A正確;
B.由圖可知P(HCl)g=0.25MPa,溫度從300℃升高到500℃時MgCl2•6H2O晶體由Mg(OH)Cl轉變成MgO,故B錯誤;
C.加熱MgCl2•6H2O晶體,P(HCl)g較小,鎂離子水解生成氫氧化鎂,得不到氯化鎂,若要得到無水氯化鎂,則應通入HCl,而增大P(HCl)g,抑制鎂離子的水解,故C錯誤;
D.由圖可知在HCl氣體壓強為0.25×106Pa時,溫度由室溫升高至300℃,發生的反應為MgCl2•6H2O═Mg(OH)Cl+HCl+5H2O,故D正確;
故答案為:AD;
(3)根據圖象曲線變化可知,反應①、③為放熱反應,隨著溫度的升高,平衡常數K逐漸減小,則lgK逐漸減小,而反應②為吸熱反應,升高溫度,平衡常數K逐漸增大,則lgK逐漸增大,所以Ⅰ表示的為反應③、Ⅱ曲線表示的為反應②,變化規律為:當△H>0時,lgK隨溫度升高而增大,當△H<0時,lgK隨溫度升高而減小;根據反應①和曲線Ⅰ(反應③反應)的反應熱可知,當溫度同等變化時,△H的數值越大lgK的變化越大,
故答案為:當△H>0時,lgK隨溫度升高而增大,當△H<0時,lgK隨溫度升高而減小;當溫度同等變化時,△H的數值越大lgK的變化越大;(或△H的數值越大,lgK隨溫度的變化程度越大).
點評 本題考查較為綜合,涉及物質的量隨時間變化的曲線、化學平衡及其影響、化學平衡狀態的判斷等知識,試題知識點較多、綜合性較強,充分考查學生的分析、理解能力及靈活應用能力.


 暑假作業海燕出版社系列答案
暑假作業海燕出版社系列答案 本土教輔贏在暑假高效假期總復習云南科技出版社系列答案
本土教輔贏在暑假高效假期總復習云南科技出版社系列答案 暑假作業北京藝術與科學電子出版社系列答案
暑假作業北京藝術與科學電子出版社系列答案科目:高中化學 來源: 題型:選擇題
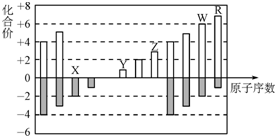
| A. | 離子半徑:X>Y>Z | |
| B. | WX3和水反應形成的化合物是離子化合物 | |
| C. | 最高價氧化物對應的水化物酸性:R>W | |
| D. | Y和Z兩者最高價氧化物對應的水化物能相互反應 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①③ | B. | ②④ | C. | ①④ | D. | ②③ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | VA=3.0mol•L-1•min-1 | B. | VB=0.2mol•L-1•s-1 | ||
| C. | VC=4.8mol•L-1•min-1 | D. | VD=4.0mol•L-1•min-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 生物質資源是一種污染小的可再生能源,可由其制得多種化工原料,如甲醛、甲醇和二甲醚等.
生物質資源是一種污染小的可再生能源,可由其制得多種化工原料,如甲醛、甲醇和二甲醚等.| 容器 | 甲 | 乙 | 丙 |
| 反應物投入量 | 1molCO、2molH2 | 1mol CH3OH | 2molCO、4molH2 |
| CH3OH平衡時濃度(mol/L) | c1 | c2 | c3 |
| 反應的能量變化 | 放出Q1kJ | 吸收Q2kJ | 放出Q3kJ |
| 平衡常數 | K1 | K2 | K3 |
| 反應物轉化率 | a1 | a2 | a3 |
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:實驗題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | A | B | C | D |
| n(CO2)(mol) | 6 | 4 | 3 | 2 |
| n(沉淀)(mol) | 2 | 3 | 2 | 1 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com