
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ① | ⑩ | ||||||
| 2 | ⑥ | ⑦ | ||||||
| 3 | ② | ③ | ④ | ⑧ | ||||
| 4 | ⑤ | ⑨ |
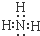 .
.分析 由元素在周期表中的位置可知,①為H、②為Na、③為Mg、④為Al、⑤為K、⑥為C、⑦為F、⑧為Cl、⑨為Br、⑩為He.
(1)稀有氣體原子最外層為穩定結構,化學性質最不活潑;
(2)金屬性越強,最高價氧化物對應水化物的堿性越強;
(3)同主族自上而下原子半徑增大;
(4)同主族自上而下非金屬性減弱,非金屬性越強,氫化物越穩定;
(5)上述元素的氫化物水溶液呈堿性為NH3;
(6)Al單質能與鹽酸、氫氧化鈉反應反應,與氫氧化鈉溶液反應生成偏鋁酸鈉與氫氣.
解答 解:由元素在周期表中的位置可知,①為H、②為Na、③為Mg、④為Al、⑤為K、⑥為C、⑦為F、⑧為Cl、⑨為Br、⑩為He.
(1)稀有氣體He原子最外層為穩定結構,化學性質最不活潑,故答案為:He;
(2)金屬性Na>Mg>Al,金屬性越強,最高價氧化物對應水化物的堿性越強,故NaOH的堿性最強,含有離子鍵、共價鍵,故答案為:NaOH;離子鍵、共價鍵;
(3)同主族自上而下原子半徑增大,故原子半徑:K>Na>H,故答案為:K>Na>H;
(4)同主族自上而下非金屬性減弱,非金屬性越強,氫化物越穩定,故氫化物穩定性:HF>HCl>HBr,故答案為:HF>HCl>HBr;
(5)上述元素的氫化物水溶液呈堿性為NH3,電子式為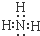 ,故答案為:
,故答案為: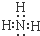 ;
;
(6)上述元素中Al單質能與鹽酸、氫氧化鈉反應反應,與氫氧化鈉溶液反應生成偏鋁酸鈉與氫氣,反應離子方程式為2Al+2OH-+2H2O═2AlO2-+3H2↑,
故答案為:Al;2Al+2OH-+2H2O═2AlO2-+3H2↑.
點評 本題考查元素周期律與元素周期表,難度不大,側重對基礎知識的鞏固,需要學生熟練掌握基礎知識,注意對元素周期律的理解應用.


科目:高中化學 來源: 題型:選擇題
| A. | 濃硝酸使紫色石蕊試液先變紅后褪色--酸性和強氧化性 | |
| B. | 不能用稀硝酸與鋅反應制氫氣--強氧化性 | |
| C. | 要用棕色瓶盛裝濃硝酸--不穩定性 | |
| D. | 稀硝酸能使滴有酚酞的氫氧化鈉溶液紅色褪去--強氧化性 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 加成-消去-取代 | B. | 消去-加成-取代 | C. | 取代-消去-加成 | D. | 取代-加成-消去 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 18O與19F具有相同的中子數 | |
| B. | 16O與17O具有相同的電子數,互為同位素 | |
| C. | 15N與14N具有相同的質子數,是同種核素 | |
| D. | 12C與13C具有不同的質量數,屬于同種元素 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | A原子電子層數比B原子的電子層數多 | |
| B. | 常溫時,A能從稀酸中置換出氫,而B不能 | |
| C. | A原子最外層電子數比B原子的最外層電子數少 | |
| D. | 1molA從酸中置換生成的H2比1mol B從酸中置換生成的H2多 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 石蕊溶液呈藍色的溶液:K+、Na+、NO3-、Cl- | |
| B. | 無色透明溶液中:MnO4-、K+、Na+、NO3- | |
| C. | 與鋁反應產生大量氫氣的溶液:Na+、K+、NH4+、NO3- | |
| D. | 酸性溶液中:Al3+、Na+、SO42-、HCO3- |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 在水溶液中能導電的化合物都是電解質 | |
| B. | 在熔融狀態下不導電的化合物都是非電解質 | |
| C. | 氨水為混合物,不屬于電解質 | |
| D. | 硫酸溶于水能導電,所以濃硫酸為電解質 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 原子半徑:F>Cl>Br | B. | 最外層電子數都相同 | ||
| C. | 核外電子層數都相同 | D. | 最外層電子數依次增多 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
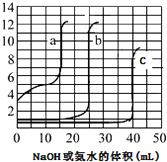 取未知濃度的硫酸、鹽酸和醋酸各25.00mL,分別用0.10mol•L-1的NaOH溶液或0.10mol•L-1 的稀氨水滴定得如圖.下列說法正確的是( )
取未知濃度的硫酸、鹽酸和醋酸各25.00mL,分別用0.10mol•L-1的NaOH溶液或0.10mol•L-1 的稀氨水滴定得如圖.下列說法正確的是( )| A. | 由圖可知曲線c為NaOH滴定硫酸 | |
| B. | 由圖可知硫酸的物質的量濃度大于鹽酸的物質的量濃度 | |
| C. | 曲線b、c的滴定實驗可用酚酞做指示劑 | |
| D. | 由圖可知滴定前醋酸電離度約為1.67% |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com