
物質的結構決定物質的性質。請回答下列涉及物質結構和性質的問題:
(1)第二周期中,元素的第一電離能處于B與N之間的元素有_________種。
(2)某元素位于第四周期Ⅷ族,其基態原子的未成對電子數與基態碳原子的未成對電子數相同,則其基態原子的價層電子排布式為_________________
(3)乙烯酮(CH2=C=O)是一種重要的有機中間體,可用CH3COOH在(C2H5O)3P=O存在下加熱脫H2O得到。乙烯酮分子中碳原子雜化軌道類型是_____________,1mol (C2H5O)3P=O分子中含有的σ鍵與π鍵的數目比為__________________。
(4)已知固態NH3、H2O、HF的氫鍵鍵能和結構如下:
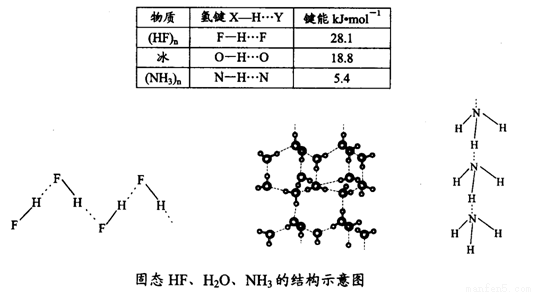
解釋H2O、HF、NH3沸點依次降低的原因___________________。
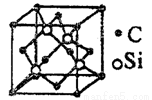
(5)碳化硅的結構與金剛石類似(如圖所示),其硬度僅次于金剛石,具有較強的耐磨性能。碳化硅晶胞結構中每個碳原子周圍與其距離最近的硅原子有___________個,與碳原子等距離最近的碳原子有__________個。已知碳化硅晶胞邊長為a pm,則碳化硅的密度為__________g·cm3。
科目:高中化學 來源:2015-2016學年河北省冀州市高一下期末理科化學A卷(解析版) 題型:選擇題
蘋果酸是一種常見的有機酸,其結構簡式如下圖。蘋果酸可能發生的反應是 ( )
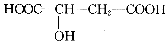
①NaOH溶液反應
②使石蕊溶液變紅
③與金屬鈉反應放出氣體
④一定條件下與乙酸發生酯化反應
⑤一定條件下與乙醇發生酯化反應
A.①②③ B.①②③④ C.①②③⑤ D.①②③④⑤
查看答案和解析>>
科目:高中化學 來源:2015-2016學年河北省冀州市高一下期末理科化學A卷(解析版) 題型:選擇題
近來,科學家研制了一種新型的乙醇電池(DEFC),它用磺酸類質子作溶劑,在200℃左右時供電,乙醇電池比甲醇電池效率高出32倍且更加安全.電池總反應式為:C2H5OH+3O2→2CO2+3H2O.下列說法不正確的是( )
A.C2H5OH在電池的負極上參加反應
B.1mol乙醇被氧化轉移6mol電子
C.在外電路中電子由負極沿導線流向正極
D.電池正極得電子的物質是O2
查看答案和解析>>
科目:高中化學 來源:2015-2016學年河北省冀州市高一下期末理科化學A卷(解析版) 題型:選擇題
化學能與熱能、電能等可以相互轉化.關于化學能與其他能量相互轉化的說法正確的是( )
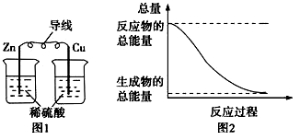
A.圖1 所示的裝置能將化學能轉變為電能
所示的裝置能將化學能轉變為電能
B.圖2所示的反應為吸熱反應
C.中和反應中,反應物的總能量比生成物的總能量低
D.化學反應中能量變化的主要原因是化學鍵的斷裂與生成
查看答案和解析>>
科目:高中化學 來源:2016屆福建省高三下熱身考理綜化學試卷(解析版) 題型:選擇題
25℃時,將濃度均為0.1mol·L-1HX溶液和HY溶液分別與等濃度的NaHCO3溶液等體積混合,實驗測得產生的氣體體積(V)隨時間(t)變化的示意圖如圖所示:下列說法正確的是
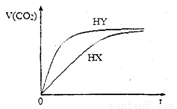
A.相同濃度的HX和HY溶液中水的電離程度:HX﹥HY
B.相同體積相同濃度的HX和HY溶液中陰離子數目前者大于后者
C.向10 mL 0.1 mol·L -1的Na2CO3溶液中緩慢滴加10 mL 0.1 mol·L -1的HY,混合后的離子濃度大小關系:c(Na+)﹥c(Y-)﹥c(HCO3-)﹥c(OH-)﹥c(H+)
D.將等體積等濃度的HX和HY溶液分別用相同濃度的氫氧化鈉溶液滴定,至中性時,消耗的氫氧化鈉溶液體積前者大于后者
查看答案和解析>>
科目:高中化學 來源:2016屆福建省高三下模擬考試理綜化學試卷(解析版) 題型:簡答題
煤的綜合利用對于改善大氣質量和能源充分利用有重要的意義。
(1)下列說法正確的是 (填序號)。
a.煤是由有機物和少量無機物組成的復雜混合物
b.煤在燃燒過程中會生成一氧化碳、二氧化碳、氮氧化物、煙塵等有害物質
c.可利用生石灰、熟石灰、石灰石等固硫劑使煤在燃燒過程中生成穩定的硫酸鹽
d.煤的干餾屬于化學變化,煤的氣化和液化都屬于物理變化
(2)煤的氣化過程中產生的有害氣體H2S用氨水吸收生成正鹽的離子方程式是
。
(3)燃煤煙氣的一種脫硫方案-火堿-石灰-石膏法流程圖1如下:
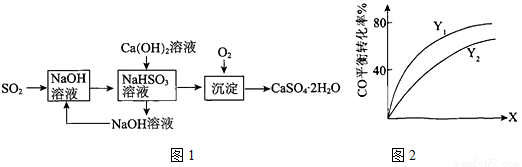
①常溫下,用NaOH溶液吸收SO2得到pH=6的NaHSO3溶液,該溶液中離子濃度的大小順序是
。
②氫氧化鈣與NaHSO3反應的化學方程式是 。
(4)煤的間接液化法合成二甲醚的三步反應如下:
Ⅰ.2H2(g)+CO(g)  CH3OH(g) △H=-90.8kJ·mol-1
CH3OH(g) △H=-90.8kJ·mol-1
Ⅱ.2CH3OH(g)  CH3OCH3(g)+ H2O(g) △H=-23.5 kJ·mol-1
CH3OCH3(g)+ H2O(g) △H=-23.5 kJ·mol-1
Ⅲ.CO(g) + H2O(g)  CO2(g) + H2(g) △H=-41.3 kJ·mol-1
CO2(g) + H2(g) △H=-41.3 kJ·mol-1
① 總反應熱化學方程式:3H2(g)+ 3CO(g)  CH3OCH3(g)+ CO2(g) △H=
CH3OCH3(g)+ CO2(g) △H=
② Y(Y1、Y2),X可分別代表壓強或溫度。如圖2表示Y一定時,總反應中CO的平衡轉化率隨X的變化關系。判斷Y1、Y2的大小關系,并簡述理由:
。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年江蘇省高二下第二次月考化學試卷(解析版) 題型:選擇題
橙花醇具有玫瑰及蘋果香氣,可作為香料,其結構簡式如下
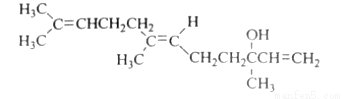
下列關于橙花醇的敘述,正確的是
A.橙花醇的分子式為C15H24O
B.在濃硫酸催化下加熱脫水,可以生成不止一種四烯烴
C.在一定條件下能發生取代、催化氧化、酯化、加聚反應
D.0.1mo1橙花醇在室溫下與溴的四氯化碳溶液反應,最多消耗0.3mo1Br2
查看答案和解析>>
科目:高中化學 來源:2015-2016學年山西省高二5月月考化學試卷(解析版) 題型:簡答題
CO2加氫合成甲醇的技術,對減少溫室氣體排放和減緩燃料危機具有重要意義,發生的主要反應如下:CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
回答下列問題:
(1)已知:H2和CH3OH的燃燒熱分別為-285.8kJ·mol-1,-726.51kJ·mol-1;以及H2O(l)=H2O(g) △H=+44kJ·mol-1;則該反應的△H=________________;
(2)該反應的平衡常數表達式為________________;
(3)在350℃時,體積為0.5L的密閉容器中,充入1molCO2和3molH2發生上述反應,測定出CH3OH的體積分數隨時間變化的曲線如圖所示:

①能判斷該反應達到化學平衡狀態的依據是__________________;
A.容器內壓強不變 B.H2的體積分數不變 C.c(CH3OH)=c(H2O) D.容器內密度不變
②氫氣在0~10min的平衡反應速率v(H2)=_________________________;
③在右圖中標出400℃時CH3OH的體積分數隨時間變化的曲線。
(4)科學家預言,燃料電池將是21世紀獲得電力的重要途徑,美國已計劃將甲醇燃料用于軍事目的。一種甲醇燃料電池是采用鉑或碳化鎢作電極催化劑,在稀硫酸電解液中直接加入純化后的甲醇,同時向另一個電極通入空氣。試回答下列問題:

①這種電池放電時,b處通入______________,發生的電極反應方程式是_____________________。
②若電解液中的3molH+通過質子交換膜,則消耗甲醇__________L(標準狀況)。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com