
碘缺 乏病是目前已知的導致人類智力障礙的主要原因。為解決這一全國性問題,我國已經開始實施“智力工程”,最經濟可行的措施是
乏病是目前已知的導致人類智力障礙的主要原因。為解決這一全國性問題,我國已經開始實施“智力工程”,最經濟可行的措施是
A.食鹽加碘(鹽) B.面包加碘(鹽)
C.大量食用海帶 D.注射含碘藥劑
科目:高中化學 來源:2016-2017學年湖北省蘄春縣高二上學期期中化學試卷(解析版) 題型:填空題
T℃時,在2L恒容密閉容器中氣態物質X、Y、Z的物質的量隨時間變化的部分數據如表所示:
T/min | n(X) /mol | n(Y) /mol | n(Z) /mol |
0 | 0.80 | 1.00 | 0 |
1 | 0.70 | 0.80 | 0.20 |
5 | 0.70 | ||
9 | 0.40 | ||
10 | 0.40 | 0.80 |
(1)寫出該反應的化學方程式_________________
(2)反應進行到10min,X的轉化率為___________,0~5min內Y的平均反應速率為___________
(3)計算T℃時該反應的平衡常數K=____________
(4)T℃下向該密閉容器中通入一定量的X、Y、Z,反應到某時刻測得X、Y、Z的物質的量分別為1.00mol、0.50mol、1.60mol,則此時正逆反應速率大小:v正 v逆(填“大于”、“等于”、“小于”)
(5)若在10min和t3、t5時刻分別改變該反應的某一反應條件,得到X、Z的物質的量及反應速率與時間的關系如下圖A、B所示:
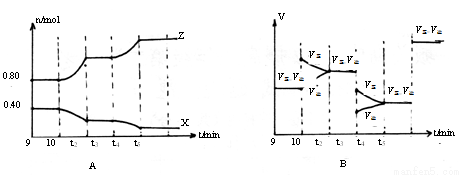
10min時改變的反應條件是_______________
②t3時刻改變的反應條件是_______________
③t5時刻改變的反應條件是 ,理由是___________________
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山東省菏澤市高二上學期期中化學試卷(解析版) 題型:填空題
在100℃時,將0.200mol的四氧化二氮氣體充入2L抽空的密閉容器中,每隔一定時間對該容器內的物質進行分析,得到如下表格:
時間(S) | 0 | 20 | 40 | 60 | 80 | 100 |
c(N2O4)mol | 0.200 | c1 | 0.10 | c3 | a | b |
c(NO2)mol | 0.000 | 0.120 | c2 | 0.240 | 0.240 | 0.240 |
試填空:(1)該反應的化學方程式為_______________,
(2)達到平衡時四氧化二氮的轉化率為__________________。
(3)20s時四氧化二氮的濃度c1=_____________mol·L-1,
(4)在0~20s時間段內,二氧化氮的平均反應速率為_____________。
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山東省菏澤市高二上學期期中化學試卷(解析版) 題型:選擇題
下列有關化學反應速率的敘述中,正確的是( )
A.100mL2mol/L的鹽酸與鋅反應時,加入適量的氯化鈉溶液,生成氫氣的速率不變
B.用鐵片和稀硫酸反應制取氫氣時,改用鐵片和濃硫酸可以加快產生氫氣的速率
C.汽車尾氣中的CO和NO可以緩慢反應生成N2和CO2,加入催化劑,不影響CO的轉化率
D.二氧化硫的催化氧化是一個放熱反應,升高溫度,平衡逆向移動,正反應速率減慢
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山東省濱州市鄒平縣高二上學期期中化學試卷(解析版) 題型:實驗題
糖類、蛋白質是基本的營養物質,在我們的生活中扮演著及其重要的角色。如何識別這些物質的真偽,既可以檢驗同學們將化學知識與實際相結合的能力水平,又可以減少偽劣物品對我們生活質量的負面影響。請根據下列的實驗現象填寫下表:
①燒焦羽毛味;②藍色;③銀鏡(析出銀);④磚紅色沉淀;⑤黃色
被鑒別的物質 | 鑒別物質(或鑒別方法) | 現象(填入序號即可) |
葡萄糖 | 新制氫氧化銅 | |
淀 粉 | 碘 水 | |
蛋白質 | 濃硝酸 | |
蛋白質 | 燃 燒 | |
葡萄糖 | 銀氨溶液 |
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山東省濱州市鄒平縣高二上學期期中化學試卷(解析版) 題型:選擇題
某人在檢查身體時,發現尿液呈微酸性,醫生建議他
A.少吃蘋果、梨等水果
B.少吃菠菜、芹菜等蔬菜
C.少喝牛奶、豆汁等飲料
D.少吃含蛋白質、脂肪多的肉類食品
查看答案和解析>>
科目:高中化學 來源:2016-2017學年山東省濱州市鄒平縣高二上學期期中化學試卷(解析版) 題型:選擇題
下列方法適宜于軟化永久硬水的是
A.離子交換法 B.長時間加熱
C.加入Na2SO4 D.加入AgNO3
查看答案和解析>>
科目:高中化學 來源:2016-2017學年內蒙古高二上學期期中化學試卷(解析版) 題型:選擇題
下列關系的表述中,正確的是( )
A.0.1mol· L-1NaHSO4溶液中:c(Na+)+c(H+)=c(SO42-)+c(OH-)
B.中和pH和體積都相同的鹽酸和醋酸,消耗NaOH的物質的量之比為1:1
C.pH=3的鹽酸和pH=3的FeCl3溶液中,由水電離出的c(H+)相等
D.0.1mol· L-1NaHCO3溶液中:c(Na+)>c(HCO3)>c(H2CO3)>c(CO32-)
查看答案和解析>>
科目:高中化學 來源:2016-2017學年四川省高二上期中化學卷(解析版) 題型:填空題
根據題意回答問題:
(1)中和熱的測定所需的玻璃儀器有:大小燒杯、量筒、溫度計、 ;
已知:0.55 mol·L-1 HCl和0.50 mol·L-1的NaOH溶液各50 mL反應放出熱量為1.42kJ,寫出該反應的中和熱的熱化學方程式: 。
(2)101kpa時,1克乙醇(CH3CH2OH)液體完全燃燒生成穩定氧化物放出熱量akJ,寫出乙醇燃燒熱的熱化學方程式: 。
(3)已知H-H、O=O和O-H鍵的鍵能分別為436 kJ/mol、498 kJ/mol和463 kJ/ mol,2H2O(g) = 2H2(g)+ O2(g) ΔH2= 。
mol,2H2O(g) = 2H2(g)+ O2(g) ΔH2= 。
(4)用CO2和氫氣合成CH3OCH3(甲醚)是解決能源危機的研究方向之一。
已知:CO(g)+2H2(g  CH3OH(g) ΔH=-90.7 kJ·mol-1
CH3OH(g) ΔH=-90.7 kJ·mol-1
2CH3OH(g  CH3OCH3(g)+H2O(g) ΔH=-23.5 kJ·mol-1
CH3OCH3(g)+H2O(g) ΔH=-23.5 kJ·mol-1
CO(g)+H2O(g  CO2(g)+H2(g) ΔH=-41.2 kJ·mol-1
CO2(g)+H2(g) ΔH=-41.2 kJ·mol-1
則CO2和氫氣合成CH3OCH3(g)的熱化學方程式為: 。
(5)① 25℃時,濃度均為0.1 mol/L的①氨水②氫氧化鈉溶液③鹽酸溶液④醋酸溶液,其c(H+)由大到小排列的順序為: (用序號填空)。
② 95℃時,水中的H+的物質的量濃度為10-6 mol·L-1,若把0.01 mol的NaOH固體溶解于95℃水中配成1 L溶液,則溶液的pH為 。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com