
A~J分別表示中學化學中常見的一種物質,它們之間相互關系如圖所示(部分反應物、生成物沒有列出),且已知G為主族元素的固態氧化物,A、B、C、D、E、F六種物質中均含同一種元素。
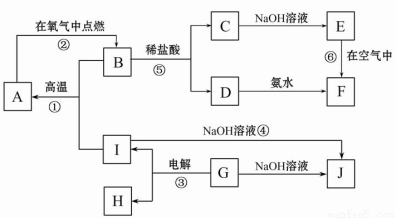
請填寫下列空白:
(1)A、B、C、D、E、F六種物質中所含的同一種元素在周期表中的位置_____________。
(2)寫出反應①、⑤、⑥的化學方程式和反應④的離子方程式。
反應①:__________________________________
反應⑤:__________________________________
反應⑥:__________________________________
反應④:__________________________________
(3)從能量變化的角度看,①、②、③反應中,ΔH<0的是____________(填序號)。
 口算小狀元口算速算天天練系列答案
口算小狀元口算速算天天練系列答案科目:高中化學 來源:2015-2016學年山東省淄博市高二上學期期中測試化學試卷(解析版) 題型:選擇題
已知:Na2O2(s)+CO2(g) Na2CO3(s) +
Na2CO3(s) +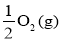 ΔH=-226 kJ/mol
ΔH=-226 kJ/mol
2CO(g)+O2(g) 2CO2(g) ΔH=-566 kJ/mol
2CO2(g) ΔH=-566 kJ/mol

 根據以上熱化學方程式判斷,下列說法正確的是
根據以上熱化學方程式判斷,下列說法正確的是
 A.CO的燃燒熱為283 kJ
A.CO的燃燒熱為283 kJ
B.2Na2O2(s)+2CO2(g) =2Na2CO3(s)+O2(g) ΔH=+452 kJ/mol
C.右圖可表示由CO生成CO2的反應過程和能量關系
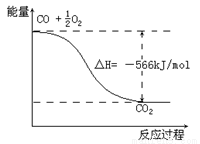
D.CO(g)與Na2O2(s)反應生成1molNa2CO3(s)時放出509kJ的熱量
查看答案和解析>>
科目:高中化學 來源:2016屆江蘇省淮安市高三上學期11月月考化學試卷(解析版) 題型:填空題
Ⅰ.甲醇來源豐富、價格低廉、運輸貯存方便,是一種重要的化工原料,有著重要的用途和應用前景。
(1)工業生產甲醇的常用方法是CO(g)+2H2(g)===CH3OH(g) ΔH=-90.8 kJ·mol-1。
已知:2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ·mol-1
H2(g)+1/2O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1
①H2的燃燒熱ΔH=___________kJ·mol-1。
②CH3OH(g)+O2(g)===CO(g)+2H2O(g)的反應熱ΔH=________________。
(2)工業上利用甲醇制備氫氣常用方法之一是甲醇蒸氣重整法。該法中的一個主要反應為CH3OH(g)===CO(g)+2H2(g),此反應能自發進行的原因是____________________________。
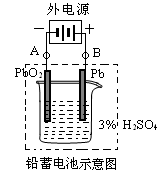
Ⅱ.鉛蓄電池是典型的可充型電池,它的正負極格板是惰性材料,電池總反應式為:
Pb+PbO2+4H++2SO42- 2PbSO4+2H2O
2PbSO4+2H2O
請回答下列問題(不考慮氫、氧的氧化還原):
(1)放電時:正極的電極反應式是________________;當外電路通過1 mol電子時,理論上負極板的質量增加________g。
(2)在完全放電耗盡PbO2和Pb時,若按圖連接,電解一段時間后,則在A電極上生成________、B電極上生成________。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年黑龍江省高二上一次月考化學試卷(解析版) 題型:選擇題
已知HA的酸性比HB的酸性強。現有物質的量濃度和體積均相同的NaA和NaB兩種溶液,已知前者溶液中離子數目為n1,后者溶液中離子數目為n2。下列關系正確是
A. n1=n2 B. n1>n2
C. n1<n2 D.c(A—)<c(B—)
查看答案和解析>>
科目:高中化學 來源:2015-2016學年黑龍江哈爾濱六中高一10月月考化學試卷(解析版) 題型:選擇題
由CH4和O2組成的混合氣體,標準狀況下的密度為1 g·L-1,則該混合氣體中CH4和O2的體積比為
A.2 : 1 B.1 : 2
C.2 : 3 D.3 : 2
查看答案和解析>>
科目:高中化學 來源:2016屆山東省高三上學期10月教學質檢理綜化學試卷(解析版) 題型:推斷題
A、B、C、D、E、X是中學常見的無機物,存在如下圖轉化關系(部分生成物和反應條件略去)。
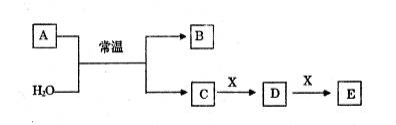
(1)若A為常見的金屬單質,焰色反應呈黃色,X能使品紅溶液褪色,寫出C和E反應的離子方程式:_______________________。
(2)若A為短周期元素組成的單質,該元素的最高價氧化物的水化物酸性最強,則:
①組成單質A的元素在周期表中的位置為______________________。
②X可能為__________________(填代號)。
a.NaHCO3 b.Na2CO3 c.Na2SO3 d.Al(OH)3
(3)若A為淡黃色粉末,回答下列問題:
①A與H2O反應的氧化產物為_____________。
②若X為非金屬單質,通常為黑色粉末,寫出E的化學式______________。
③若X為一種造成溫室效應的氣體。則鑒別等濃度的D、E兩種溶液,可選擇的試劑為___________(填代號)。
a.鹽酸 b.BaCl2溶液 c.NaOH溶液 d.Ca(OH)2溶液
(4)若A為氧化物,X是Fe,溶液D中加入KSCN溶液變紅。
①A與H2O反應的化學反應方程式為____________________________。
②檢驗溶液D中還可能存在Fe2+的方法是____________________________(注明試劑、現象)。
查看答案和解析>>
科目:高中化學 來源:2016屆山東省臨沂市高三上學期10月階段性教學質檢化學試卷(解析版) 題型:選擇題
化學與生產、生活密切相關。下列說法錯誤的是
A.“硅膠”常用作袋裝食品的干燥劑
B.氫氧化鋁具有弱堿性,常用作胃酸中和劑
C.碳纖維,是一種新型無機非金屬材料
D.工業上以氯氣和澄清石灰水為原料制造漂白粉
查看答案和解析>>
科目:高中化學 來源:2016屆四川省德陽市高三上學期10月月考理綜化學試卷(解析版) 題型:選擇題
向分別含SO32-、Fe2+、Br-、I-各0.1mol的溶液中,通入標準狀況下的Cl2,通入Cl2的體積和溶液中相關離子的物質的量關系圖正確的是:
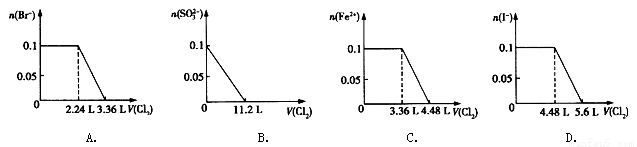
查看答案和解析>>
科目:高中化學 來源:2016屆浙江省新安江校區高三上學期第二次模擬化學試卷(解析版) 題型:選擇題
已知部分弱酸的電離平衡常數如下表:
弱酸 | 醋酸 | 次氯酸 | 碳酸 | 亞硫酸 |
電離平衡常數(25℃) | Ka=1.75ⅹ10-5 | Ka=2.98ⅹ10-8 | Ka1=4.3ⅹ10-7 Ka2=5.61ⅹ10-11 | Ka1=1.54ⅹ10-2 Ka2=1.02ⅹ10-7 |
下列離子方程式正確的是
A.少量的CO2通入NaClO溶液中:CO2+H2O+2ClO-=CO32-+2HclO
B.少量的SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO
C.少量的SO2通入Na2CO3溶液中:SO2+H2O+2CO32-=SO32-+2HCO3-
D.相同濃度的NaHCO3溶液與NaHSO3溶液等體積混合:H++ HCO3-=CO2↑+2H2O
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com