
分析 (1)分子結構為正四面體的為四氯化碳;常用分餾的方法分離;
(2)CF3CHClBr對應的同分異構體中,可根據鹵素原子的位置不同判斷;
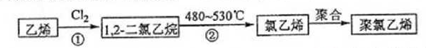
(3)乙烯與氯氣發生加成反應生成1,2-二氯乙烷,加熱480~530℃生成氯乙烯,然后發生加聚反應可生成聚氯乙烯.
解答 解:(1)分子結構為正四面體的為四氯化碳,工業上分離這些多氯代甲烷,根據物質的沸點不同,常用分餾的方法分離,
故答案為:四氯化碳;分餾;
(2)CF3CHClBr對應的同分異構體中,可根據鹵素原子的位置不同判斷,如F不在同一個C原子上,存在的同分異構體有:CHFClCF2Br、CHFBrCF2Cl、CFClBrCHF2,
故答案為:CHFClCF2Br、CHFBrCF2Cl、CFClBrCHF2;
(3)乙烯與氯氣發生加成反應生成1,2-二氯乙烷,反應的方程式為H2C=CH2+Cl2→CH2ClCH2Cl,加熱480~530℃生成氯乙烯,發生消去反應,
故答案為:H2C=CH2+Cl2→CH2ClCH2Cl;加成反應;消去反應.
點評 本題綜合考查鹵代烴的組成、結構和性質,題目難度中等,側重于學生的分析能力的考查,注意把握有機物的官能團的性質以及同分異構體的判斷.


科目:高中化學 來源: 題型:解答題
| 溫度/℃ | 400 | 500 | 800 |
| 平衡常數K | 9.94 | 9 | 1 |
| 實驗序號 | 反應溫度/℃ | H2C2O4溶液 | 酸性KMO4溶液 | H2O | ||
| V/mL | c/(mol•L-1) | V/mL | c/(mol•L-1) | V/mL | ||
| ① | 25 | 8.0 | 0.20 | 5.0 | 0.010 | 0 |
| ② | 25 | 6.0 | 0.20 | 5.0 | 0.010 | x |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
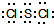 ,它在常溫下呈液態,形成晶體時,屬于
,它在常溫下呈液態,形成晶體時,屬于查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 1 mol R(g)的能量總和大于1 mol M(s)與1 mol N(g) 的能量總和 | |
| B. | 將2 mol R (g)與1 mol N(g)在該條件下充分反應,放出熱量Q2 kJ | |
| C. | 當1 mol M(s) 與N(g)完全轉化為T (g)時(假定無熱量損失),放出熱量Q1+$\frac{{Q}_{2}}{2}$kJ | |
| D. | M(g)+N(g)?R(g)△H=-Q3 kJ•mol-1,則Q3<Q1 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
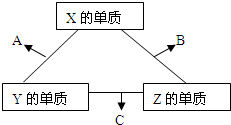
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
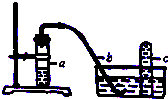 實驗室用如圖裝置,利用Cu與HNO3反應來制取NO并用排水法收集氣體.
實驗室用如圖裝置,利用Cu與HNO3反應來制取NO并用排水法收集氣體.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | s能級原子軌道呈球形,其電子運動軌跡呈球形 | |
| B. | P能級軌道數隨電子層數遞增而增多 | |
| C. | 在基態多電子原子中,N層上的電子能最一定比M層上的高 | |
| D. | 在基態多電子原子中,不可能有兩個運動狀態完全相同的電子 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
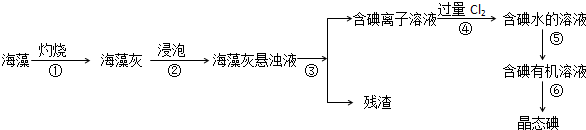
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com