
【題目】(1)H2A在水中存在以下平衡:H2A![]() H++HA-,HA-
H++HA-,HA-![]() H++A2-。NaHA溶液顯酸性,則溶液中離子濃度的大小順序為__________________________。
H++A2-。NaHA溶液顯酸性,則溶液中離子濃度的大小順序為__________________________。
(2)已知常溫下H2A的鈣鹽(CaA)飽和溶液中存在以下平衡:CaA(s)![]() Ca2+(aq)+A2-(aq)滴加少量Na2A固體,c(Ca2+)___(填“增大”“減小”或“不變”),原因是______。
Ca2+(aq)+A2-(aq)滴加少量Na2A固體,c(Ca2+)___(填“增大”“減小”或“不變”),原因是______。
(3)含有![]() 的廢水毒性較大,某工廠廢水中含4.00×10-3 mol·L-1的Cr2O
的廢水毒性較大,某工廠廢水中含4.00×10-3 mol·L-1的Cr2O![]() 。為使廢水能達標排放,作如下處理:
。為使廢水能達標排放,作如下處理:![]()
![]() Cr2+、Fe3+
Cr2+、Fe3+![]() Cr(OH)3、Fe(OH)3
Cr(OH)3、Fe(OH)3
①該廢水中加入FeSO4·7H2O和稀硫酸,發生反應的離子方程式為:_______。
②若處理后的廢水中殘留的c(Fe3+)=1×10-13 mol·L-1,則殘留的Cr3+的濃度為__________________。{已知:Ksp[Fe(OH)3]≈1.0×10-38 ,Ksp[Cr(OH)3]≈1.0×10-31}
【答案】c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)減小加少量Na2A固體,A2-濃度增大,CaA的溶解平衡向左移動,所以c(Ca2+)減小Cr2O![]() +14H++6Fe2+===2Cr3++6Fe3++7H2O1×10-6 mol·L-1
+14H++6Fe2+===2Cr3++6Fe3++7H2O1×10-6 mol·L-1
【解析】
(1) H2A在水中存在以下平衡:H2A![]() H++HA-,HA-
H++HA-,HA-![]() H++A2-,所以H2A 是二元弱酸,NaHA在溶液中存在電離平衡和水解平衡,溶液顯酸性,說明HA-的電離程度大于水解程度,以此分析。
H++A2-,所以H2A 是二元弱酸,NaHA在溶液中存在電離平衡和水解平衡,溶液顯酸性,說明HA-的電離程度大于水解程度,以此分析。
(2)加少量Na2A固體,A2-濃度增大,CaA的溶解平衡向左移動。
(3) ①亞鐵離子被氧化的離子方程式為Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O。
②根據Ksp[Fe(OH)3]=1.0×10-38 和Ksp[Cr(OH)3]≈1.0×10-31 可知![]() =
=![]() ,根據c(Fe3+)濃度可求出Cr3+的濃度。
,根據c(Fe3+)濃度可求出Cr3+的濃度。
(1)因為鈉離子不水解,HA-既水解又電離,所以c(Na+)>c(HA-),因為NaHA溶液顯酸性,所以HA-的電離大于水解,又因為水電離也能產生H+,所以c(H+)>c(A2-),水的電離很微弱,OH-濃度很小,所以c(A2-)>c(OH-),綜上,c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)。
因此,本題正確答案是:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)。
(2)由于加入Na2A固體,c(A2-)增大,從而導致溶解平衡左移,c(Ca2+)減小。
因此,本題正確答案是:減小;加少量Na2A固體,A2-濃度增大,CaA的溶解平衡向左移動,所以c(Ca2+)減小。
(3)Cr2O![]() 有較強氧化性,FeSO4·7H2O中Fe2+有一定的還原性,在酸性介質中發生氧化還原反應,由實驗流程可知,第①步反應中Cr2O
有較強氧化性,FeSO4·7H2O中Fe2+有一定的還原性,在酸性介質中發生氧化還原反應,由實驗流程可知,第①步反應中Cr2O![]() 在酸性條件下將Fe2+氧化為Fe3+,自身被還原為Cr3+,根據元素守恒及所處環境可知,還應有水生成,反應離子方程式為Cr2O
在酸性條件下將Fe2+氧化為Fe3+,自身被還原為Cr3+,根據元素守恒及所處環境可知,還應有水生成,反應離子方程式為Cr2O![]() +14H++6Fe2+===2Cr3++6Fe3++7H2O;
+14H++6Fe2+===2Cr3++6Fe3++7H2O;
因此,本題正確答案是:Cr2O![]() +14H++6Fe2+===2Cr3++6Fe3++7H2O。
+14H++6Fe2+===2Cr3++6Fe3++7H2O。
(4)根據Ksp[Fe(OH)3]=1.0×10-38 和Ksp[Cr(OH)3]≈1.0×10-31,若處理后的廢水中殘留的c(Fe3+)=1×10-13molL-1,![]() =
=![]() ,c(Cr3+)=
,c(Cr3+)=![]() mol/L=1×10-6molL-1。
mol/L=1×10-6molL-1。
因此,本題正確答案是:1×10-6 mol·L-1。


科目:高中化學 來源: 題型:
【題目】下列各組離子,在無色透明溶液中能大量共存的是
A.NH4+、Mg2+、SO42-、Cl-B.Na+、H+、SO32-、Cl-
C.Na+、Cu2+、SO42-、OH-D.Na+、Ca2+、Cl-、CO32-
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】某學習小組欲從工業廢釩催化劑中回收V2O5,通過分析知該廢釩催化劑的主要成分如下表:
物質 | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
質量分數/% | 2.2~29 | 2.8~3.1 | 22~28 | 60~65 | 1~2 | <1 |
他們通過查閱資料找到一種廢釩催化劑的回收工藝流程路線如下:
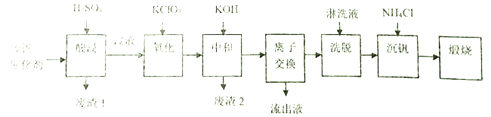
回答下列問題:
(1)“酸浸”時V2O5轉化為VO2+,V2O4轉成VO2+。則“廢渣1”的主要成分是_____________。
(2)“氧化”的目的是使VO2+變為VO2+,寫出該反應的離子方程式________________________。
(3)“中和”作用之一是使釩以V4O124-形式存在于溶液中,則“廢渣2”的成分有__________(用化學式表示)。
(4)“離子交換”和“洗脫”可簡單表示為:4ROH+ V4O124- ![]() R4V4O12+4OH-(ROH為強堿性陰離子交換樹脂)。“流出液”中陽離子最多的是_______________;為了提高洗脫效率,淋洗液應該呈______性(填“酸”、“堿“或“中”)。
R4V4O12+4OH-(ROH為強堿性陰離子交換樹脂)。“流出液”中陽離子最多的是_______________;為了提高洗脫效率,淋洗液應該呈______性(填“酸”、“堿“或“中”)。
(5)“沉釩”得到偏釩酸銨(NH4VO3)沉淀,寫出得到沉定的化學方程式__________________。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】氮的氧化物(如NO2、NO4、N2O5等)應用很廣,在一定條件下可以相互轉化。
(1) 已知:2NO(g)+O2(g)===2NO2(g) ΔH1
NO(g)+O3(g)===NO2(g)+O2(g) ΔH2
2NO2(g)![]() N2O4(g) ΔH3
N2O4(g) ΔH3
2N2O5(g)===4NO2(g)+O2(g) ΔH4
則反應N2O4(g)+O3(g)===N2O5(g)+O2(g)的ΔH=__________。
(2)從N2O5在一定條件下發生分解:2N2O5(g)===4NO2(g)+O2(g)。某溫度下測得恒容密閉容器中N2O5濃度隨時間的變化如下表:
t/min | 0.00 | 1.00 | 2.00 | 3.00 | 4.00 | 5.00 |
c(N2O5)/ (mol·L-1) | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
設反應開始時體系壓強為p0,第2.00 min時體系壓強為p,則p∶p0=________;1.00~3.00 min內,O2的平均反應速率為________。
(3)N2O4與NO2之間存在反應N2O4(g)![]() 2NO2(g)。將一定量的N2O4放入恒容密閉容器中,測得其平衡轉化率[α(N2O4)]隨溫度變化如圖所示。
2NO2(g)。將一定量的N2O4放入恒容密閉容器中,測得其平衡轉化率[α(N2O4)]隨溫度變化如圖所示。

①圖中a點對應溫度下,已知N2O4的起始壓強p0為108 kPa,列式計算該溫度下反應的平衡常數Kp=________(用平衡分壓代替平衡濃度計算,分壓=總壓×物質的量分數)。
②由圖推測N2O4(g)![]() 2NO2(g)是吸熱反應還是放熱反應,說明理由_______________,若要提高N2O4轉化率,除改變反應溫度外,其他措施有____________(要求寫出兩條)。
2NO2(g)是吸熱反應還是放熱反應,說明理由_______________,若要提高N2O4轉化率,除改變反應溫度外,其他措施有____________(要求寫出兩條)。
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】已知有機物A. B之間存在轉化關系:A(C6H12O2) +H2O![]() B+HCOOH(已配平)則符合該反應條件的有機物B有(不含立體異構)
B+HCOOH(已配平)則符合該反應條件的有機物B有(不含立體異構)
A. 6種 B. 7種 C. 8種 D. 9種
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】將標準狀況下2.24 L CO2緩慢通入1 L 0.15 mol·L-1的NaOH溶液中,氣體被充分吸收,下列關系不正確的是( )
A. 混合溶液溶質為NaHCO3和Na2CO3
B. c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-)
C. c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+)
D. 加熱蒸干所得混合溶液,最終得到Na2CO3固體
查看答案和解析>>
科目:高中化學 來源: 題型:
【題目】實驗室欲快速制取H2,應選用正確的措施是
A.純鋅與稀硫酸反應B.粗鋅跟稀硫酸反應
C.粗鋅跟硝酸反應D.將浸泡過CuSO4溶液的Zn跟稀硫酸反應
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com