
用蘸有濃氨水的棉棒檢漏輸氯管道的原理為:3Cl2+8NH3=N2+6NH4Cl。該反應的下列說法正確的是( )
A. 35.5 g氯氣所含的分子數為6.02×1023
B. 常溫常壓下,22.4 L氨氣所含原子總數為4×6.02×1023
C. 反應每生成1 mol N2轉移電子數約為6×6.02× 1023
D. 1 mol·L-1 NH4Cl溶液中,含有Cl-數約為6.02×1023
 全能測控期末小狀元系列答案
全能測控期末小狀元系列答案科目:高中化學 來源:2016-2017學年江西省景德鎮市高二(素質班)上學期期末考試化學試卷(解析版) 題型:選擇題
一定溫度下,水溶液中H+和OH-的濃度變化曲線如圖,下列說法正確的是( )
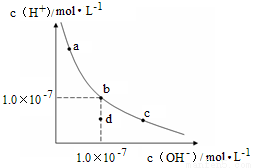
A. 升高溫度,可能引起由c向b的變化
B. 該溫度下,水的離子積常數為1.0×10-13
C. 該溫度下,加入FeCl3可能引起由b向a的變化
D. 該溫度下,稀釋溶液可能引起由c向d的變化
查看答案和解析>>
科目:高中化學 來源:2017屆廣西省高三2月份模擬演練理綜化學試卷(解析版) 題型:實驗題
氯化亞銅(CuCl)常用作有機合成工業中的催化劑。有關資料為:
①CuCl為微溶于水的白色固體,在空氣中可被迅速氧化
②CuOH為難溶于水的黃色固體,易分解為紅色的Cu2O
③Cu+可與濃氨水反應生成Cu(NH3)2+(無色),該無色物質在空氣中易被氧化為藍色
I. 甲小組同學用如下裝置電解食鹽水,并對電解產物進行研究。
實驗裝置 | 電解質溶液 | 實驗現象 | |
| 5mol/L NaCl溶液 | a極附近 | b極附近 |
開始時,產生白色渾濁并逐漸增加,當沉入U型管底部時部分沉淀變為橙黃色;隨后a極附近沉淀自下而上也變為橙黃色 | 產生無色氣泡 | ||
(1)若a極附近生成的白色渾濁是CuCl,則銅絲a應與電源的________極相連,銅絲a的電極反應式是____。
(2)b極附近溶液的pH_________(填“增大”、“減小”或“不變”)。
(3)橙黃色沉淀中含有Cu2O,則CuCl轉化為Cu2O的原因是_____________(用方程式表示)。
(4)a極附近沉淀自下而上變為橙黃色原因是____________。
II. 乙小組同學通過以下方案制取CuCl并對其組成進行研究。
將Na2SO3的水溶液逐滴加入CuCl2的水溶液中,再加入少量濃鹽酸調節到pH=3左右,即可得到白色沉淀CuCl。
(1)寫出產生CuCl的離子方程式______________。
(2)為了提高CuCl的產率,可采用________法快速過濾,生產過程中調節溶液的pH不能過大的原因是___。
(3)為探究白色沉淀的化學組成,將制得的白色沉淀溶于濃氨水,得到無色溶液,將無色溶液分成兩份,一份放置于空氣中,一段時間后溶液變為藍色;另一份的實驗方法及現象為_____________。
查看答案和解析>>
科目:高中化學 來源:2017屆山東省淄博市高三第一次模擬考試化學試卷(解析版) 題型:選擇題
下列實驗操作和理象、結論均正確且有因果關系的是
選項 | 實驗操作和現象 | 結論 |
A | 向某溶液中滴加CCl4,振蕩、靜置,下層溶液顯紫色 | 原溶液中含有I- |
B | 常溫下,0.1mol/LNaHSO3溶液的pH約為5 | HSO3-的電離程度大于其水解程度 |
C | 相同溫度下,測得飽和亞硫酸溶液的pH小于飽和碳酸溶液的pH | 亞硫酸的酸性強于碳酸 |
D | 向稀HNO3中加入過量的Fe粉,充分反應后,滴入KSCN溶液不顯紅色 | 稀HNO3將Fe氧化為Fe2+ |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化學 來源:2016-2017學年江蘇省鹽城市高二學業水平模擬(一)化學試卷(解析版) 題型:簡答題
(1)在“天宮二號”上蠶寶寶的“太空屋”形似膠囊(如圖),兩端的半球體由航天鋁合金打造,中間部分采用透明有機玻璃,蠶寶寶由聚氨酯海綿包裹著。

①蠶絲的主要成份為________(填字母)。
a. 多糖 b. 蛋白質 c. 油脂
②有機玻璃和聚氨酯海綿均屬于________(填字母)。
a. 金屬材料 b. 無機非金屬材料 c. 有機高分子材料
③鈦鋁合金是常見的航天鋁合金,下列不屬于鈦鋁合金性質的是________(填字母)。
a. 高密度 b. 高強度 c. 高韌性
品名:果肉果凍
配料表:水、白砂糖、桔子
果肉(≥15%)、魔芋粉。
食品添加劑:卡拉膠、黃原
膠、檸檬酸、氯化鉀、桔子
香精、甜密素、檸檬黃、誘
惑紅、山梨酸鉀
(2)某品牌果凍標簽如圖所示。回答下列問題:
①食品添加劑中,屬于無機鹽的是________(填化學式)。
②屬于著色劑的是誘惑紅和________;屬于防腐劑的是________。
③配料表中白砂糖的成分是蔗糖,請寫出蔗糖在人體內水解的化學方程式__________________。
(3)化學與科學技術、生產生活及環境保護等密切相關。
①2016年12月我省啟動了保衛碧水藍天的“263”行動,減少煤炭消費總量,減少霧霾天氣的發生。形成硫酸型酸雨的主要氣體是________;嚴格整治畜禽養殖場污染,主要是為減少________和P等元素及化學需氧量對水體的污染。
②目前正在推廣用尿素水解液來消除柴油汽車尾氣中的氮氧化物。寫出尿素水解液中的NH3與NO在催化劑作用下,反應生成無污染物質的化學方程式_________________。
③阿司匹林作為一種藥物,主要具有________作用;Mg2Si3O8·nH2O(三硅酸鎂)具有治療胃酸過多的作用,寫出其與胃酸反應生成SiO2·H2O等物質的化學方程式____________________。
查看答案和解析>>
科目:高中化學 來源:2016-2017學年江蘇省鹽城市高二學業水平模擬(一)化學試卷(解析版) 題型:選擇題
國產航母001A等艦艇的船底都涂有含Cu2O的防污涂料,制備Cu2O的一種方法為:Zn+2CuSO4+2NaOH===Cu2O+ZnSO4+Na2SO4+H2O。該反應的下列說法正確的是( )

A. Zn得到電子
B. CuSO4被氧化
C. NaOH是還原劑
D. CuSO4是氧化劑
查看答案和解析>>
科目:高中化學 來源:2016-2017學年江蘇省鹽城市高二學業水平模擬(一)化學試卷(解析版) 題型:選擇題
在含有大量Fe3+、H+、SO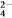 的溶液中,還可能大量共存的離子是( )
的溶液中,還可能大量共存的離子是( )
A. Ba2+ B. OH- C. I- D. NH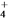
查看答案和解析>>
科目:高中化學 來源:2017屆湖北省黃岡市高三第三次聯考理綜化學試卷(解析版) 題型:選擇題
用NA表示阿伏伽德羅常數的值,下列有關說法正確的是
A. 標準狀況下,33.6LHF中含有氟原子的數目為1.5NA
B. 1.0L 1.0mol·L-1Na2SO4水溶液中含有的氧原子數為4NA
C. 電解飽和食鹽水,當陰極產生1.12LH2時,轉移的電子數為0.1NA
D. 常溫下,2L0.1mol·L-1FeCl3溶液與1L0.2mol·L-1FeCl3溶液所含Fe3+數目不同
查看答案和解析>>
科目:高中化學 來源:2017屆江蘇省常州市高三第一次模擬考試化學試卷(解析版) 題型:選擇題
常溫下,下列各組離子一定能在指定溶液中大量共存的是
A. 0.1mol/LFeC13溶液中:A13+、NH4+、Cl-、SCN-
B. 使甲基橙變紅色的溶液中:Mg2+、K+、SO42-、NO3-
C. 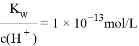 的溶液中:Na+、Fe3+、I-、AlO2-
的溶液中:Na+、Fe3+、I-、AlO2-
D. 水電離的c(H+)=1×10-13mol/L的溶液中:K+、Na+、CO32-、SO42-
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com