
| A. | 摩爾是國際科學界建議采用的一種物理量 | |
| B. | 物質的摩爾質量等于該物質的相對分子質量 | |
| C. | O22-離子的摩爾質量是32 g•mol-1 | |
| D. | 1 mol H2O的質量為18 g•mol- |
分析 A.摩爾只是物質的量的單位,不是物理量;
B.摩爾質量和相對分子質量的單位不同;
C.O22-離子的式量為32,結合摩爾質量與相對分子質量之間的關系分析;
D.質量的單位為g,g/mol為摩爾質量的單位.
解答 解:A.物質的量為基本物理量,而摩爾為物質的量的單位,故A錯誤;
B.摩爾質量的單位為g/mol,相對分子質量沒有單位,二者不相等,故B錯誤;
C.電子的質量較小,則O22-離子的式量為32,其摩爾質量是32 g•mol-1,故C正確;
D.1mol水的質量為18g,18g/mol為水的摩爾質量,故D錯誤;
故選C.
點評 本題考查了物質的量的計算,題目難度不大,明確物質的量與摩爾、摩爾質量與相對分子質量之間的關系為解答關鍵,試題側重基礎知識的考查,培養了學生的分析能力及靈活應用能力.


科目:高中化學 來源: 題型:選擇題
| A. | 15mol•L-1 | B. | 10mol•L-1 | C. | 5mol•L-1 | D. | 1mol•L-1 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 溫室效應 | B. | 氮的氧化物排放 | C. | 白色污染 | D. | 對臭氧層的破壞 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 標準狀況下,33.6 L氟化氫中含有氟原子的數目為1.5 NA | |
| B. | 常溫常壓下,7.0 g乙烯與丙烯的混合物中含有氫原子的數目為 NA | |
| C. | 50 mL 18.4 mol•L-1濃硫酸與足量銅微熱反應,生成SO2分子的數目為0.46 NA | |
| D. | 密閉容器盛有0.1 mol N2和0.3 mol H2,在一定條件下充分反應,轉移電子的數目為0.6 NA |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | ①③④⑤ | B. | ①②③⑥ | C. | ②③④⑥ | D. | ①②④⑤ |
查看答案和解析>>
科目:高中化學 來源: 題型:推斷題
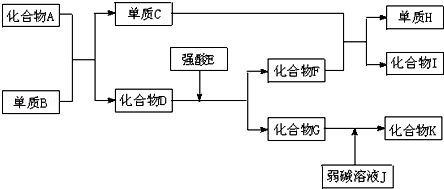
 .
.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | V(NaOH)=0時,c(H+)=1×10-2 mol/L | |
| B. | V(NaOH)=10 mL時,c(H+)=1×10-7 mol/L | |
| C. | V(NaOH)<10 mL時,可能存在c(Na+)=2c(C2O42-)+c(HC2O4-) | |
| D. | V(NaOH)>10 mL時,2c(C2O42-)>c(Na+)>c(HC2O4-) |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com