
| A. | C2H6 | B. | C2H4 | C. | C2H2 | D. | C2H6O |
分析 烴完全燃燒生成二氧化碳與水,根據碳元素守恒可知,烴含碳質量分數越大,等質量烴燃燒時生成CO2越多.
解答 解:烴完全燃燒生成二氧化碳與水,根據碳元素守恒可知,烴含碳質量分數越大,等質量烴燃燒時生成CO2越多,
A.C2H6中C、H原子數目之比為2:6=1:3;
B.C2H4中C、H原子數目之比為2:4=1:2;
C.C2H2中C、H原子數目之比為2:2=1:1;
D.C2H6O中碳質量分數小于A;
故C2H2中碳元素的質量分數最大,相同質量烴燃燒,C2H2生成二氧化碳最多,
故選:C.
點評 本題考查化學方程式計算,涉及烴燃燒反應,注意利用碳元素守恒解答,避免利用化學反應方程式的繁瑣,簡化了計算過程.


 奪冠金卷全能練考系列答案
奪冠金卷全能練考系列答案科目:高中化學 來源: 題型:選擇題

| A. | a、b不可能是同種材料的電極 | |
| B. | 該裝置可能是電解池,電解質溶液為稀H2SO4 | |
| C. | 該裝置可能是原電池,電解質溶液為稀HNO3 | |
| D. | 反應一段時間后,斷開電路,向溶液中通入H2可使溶液復原 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 化學反應 | 平衡常數 | 溫度 | |
| 973K | 1173K | ||
| ①Fe(s)+CO2(g)?FeO(s)+CO(g) | K1 | 1.47 | 2.15 |
| ②Fe(s)+H2O(g)?FeO(s)+H2(g) | K2 | 2.38 | 1.67 |
| ③CO(g)+H2O(g)?CO2(g)+H2(g) | K3 | ? | ? |
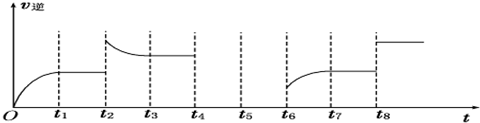
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | C(s)+$\frac{1}{2}$O2(g)=CO(g)△H=-110.5 kJ/mol | |
| B. | H2(g)+Cl2(g)=2HCl(g)△H=-184.6 kJ/mol | |
| C. | H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H=-241.8 kJ/mol | |
| D. | C8H18(l)+$\frac{25}{2}$O2(g)=8CO2(g)+9H2O(l)△H=-5518 kJ/mol |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | Cl2通入NaOH溶液中 Cl2+2OH-═Cl-+ClO-+H2O | |
| B. | 硫化亞鐵與稀硫酸反應 FeS+2H+═Fe2++H2S↑ | |
| C. | 硫酸銨和氫氧化鋇溶液 Ba2++SO42-═BaSO4↓ | |
| D. | 氫氧化鋇與稀硫酸反應 Ba2++SO42-+2H++2OH-═BaSO4↓+2H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

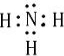 .
.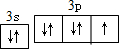 ,其單質在常溫下為黃綠色的氣體,實驗中可以用NaOH溶液吸收,反應的離子方程式為Cl2+2OH-=Cl-+ClO-+H2O.
,其單質在常溫下為黃綠色的氣體,實驗中可以用NaOH溶液吸收,反應的離子方程式為Cl2+2OH-=Cl-+ClO-+H2O.查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鋁罐可久盛食醋 | |
| B. | 氫氧化鋁可作胃酸的中和劑 | |
| C. | 鐵表而鍍鋅可以增強其抗腐蝕性 | |
| D. | 含重金屬離子的電鍍廢液不能隨意排放 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com