
分析 (1)根據反應速率v=$\frac{△c}{△t}$進行計算達到化學平衡狀態時以NH3表示的化學反應速率;
(2)根據化學反應速率與化學計量數成正比計算出用O2、NO表示的化學反應速率;
(3)根據n=vt計算出達到平衡狀態時生成NO的物質的量.
解答 解:(1)NH3的起始濃度為8mol/L,5min后達到化學平衡狀態,NH3濃度為2mol/L,則達到化學平衡狀態時以NH3表示的化學反應速率為:v=$\frac{8mol/L-2mol/L}{5min}$=1.2mol/(L•min),
答:達到化學平衡狀態時以NH3表示的化學反應速率為1.2mol/(L•min);
(2)根據反應方程式4NH3(g)+5O2(g)═4NO(g)+6H2O(g)可知,v(O2)=$\frac{5}{4}$v(NH3)=1.2mol/(L•min)×$\frac{5}{4}$=1.5mol/(L•min);
v(NO)=v(NH3)=1.2mol/(L•min),
答:用O2、NO 表示的化學反應速率分別為1.5mol/(L•min)、1.2mol/(L•min);
(3)v(NO)=v(NH3)=1.2mol/(L•min),則達到平衡時生成NO的物質的量為:n(NO)=1.2mol/(L•min)×5min=6mol,
答:達到化學平衡狀態時NO的物質的量是6mol.
點評 本題考查了化學平衡的計算,題目難度中等,明確化學反應速率與化學計量數的關系為解答關鍵,注意掌握化學反應速率的概念及表達式,試題培養了學生的分析能力及化學計算能力.


科目:高中化學 來源: 題型:選擇題
| A. | 氣體摩爾體積為22.4L/mol | B. | 1molNaOH的質量為40g | ||
| C. | 0.5molCO2的體積為11.2L | D. | H2O的摩爾質量為18g |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
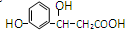 ,它不可以發生的反應類型有:①加成;②水解;③消去;④酯化;⑤銀鏡;⑥氧化;⑦取代;⑧加聚;⑨縮聚.( )
,它不可以發生的反應類型有:①加成;②水解;③消去;④酯化;⑤銀鏡;⑥氧化;⑦取代;⑧加聚;⑨縮聚.( )| A. | ①⑤⑧ | B. | ①②⑤⑨ | C. | ②⑥⑧⑨ | D. | ②⑤⑧ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 奎尼酸是制備艾滋病新藥二咖啡酰奎尼酸的原料,其結構簡式如圖,下列有關奎尼酸的說法中正確的是( )
奎尼酸是制備艾滋病新藥二咖啡酰奎尼酸的原料,其結構簡式如圖,下列有關奎尼酸的說法中正確的是( )| A. | 奎尼酸的分子式是C7H9O6 | |
| B. | 1mol奎尼酸與足量NaOH溶液反應,最多消耗NaOH物質的量為5mol | |
| C. | 1 mol奎尼酸與足量鈉反應生成56L氫氣 | |
| D. | 奎尼酸能發生消去反應,也能與乙醇、乙酸發生取代反應 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com