(2011?常州三模)工業上以黃鐵礦為原料生產硫酸主要分為三個階段進行,即煅燒、催化氧化、吸收.請回答下列個問題:
(1)煅燒黃鐵礦形成的爐氣必須經除塵、洗滌、干燥后進入
接觸室
接觸室
(填設備名稱),其主要目的是
防止催化劑中毒
防止催化劑中毒
.
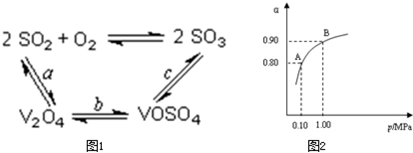
(2)催化氧化所使用的催化劑釩觸媒(V
2O
5)能加快二氧化硫氧化速率,此過程中產生了一連串的中間體(如圖1).其中a、c二步的化學方程式可表示為:
SO2+V2O5?SO3+V2O4
SO2+V2O5?SO3+V2O4
、
4VOSO4+O2?2V2O5+4SO3
4VOSO4+O2?2V2O5+4SO3
.
(3)550℃時,SO
2轉化為SO
3的平衡轉化率(α)與體系總壓強(p)的關系如圖2所示.則:將2.0mol SO
2和1.0mol O
2置于5L密閉容器中,反應達平衡后,體系總壓強為0.10M Pa.該反應的平衡常數等于
400L?mol-1
400L?mol-1
.A與B表示不同壓強下的SO
2轉化率,通常情況下工業生產中采用常壓的原因是
使用常壓SO2就可以達到較高的轉化率
使用常壓SO2就可以達到較高的轉化率
.
(4)為循環利用催化劑,科研人員最新研制了一種離子交換法回收釩的新工藝,
回收率達91.7%以上.已知廢釩催化劑中含有V
2O
5、VOSO
4及不溶性殘渣.查閱資料知:VOSO
4可溶于水,V
2O
5難溶于水,NH
4VO
3難溶于水.該工藝的流程如圖.
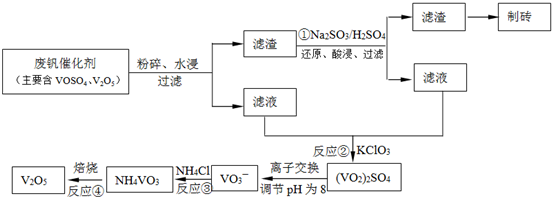
則:反應①②③④中屬于氧化還原反應的是
①②
①②
(填數字序號),反應①的離子方程式為
V2O5+SO32-+4H+=2VO2++SO42-+2H2O
V2O5+SO32-+4H+=2VO2++SO42-+2H2O
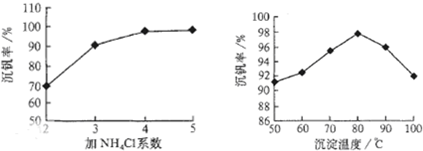
.該工藝中反應③的沉淀率(又稱沉礬率)是回收釩的關鍵之一,沉釩率的高低除受溶液pH影響外,還需要控制氯化銨系數(NH
4Cl加入質量與料液中V
2O
5的質量比)和溫度.根據下圖試建議控制氯化銨系數和度:
4
4
、
80℃
80℃
.