
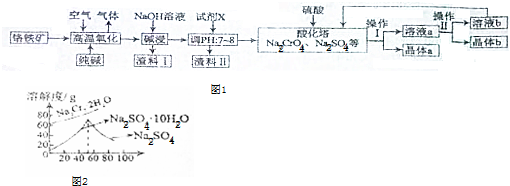
分析 鉻鐵礦(主要成分:FeO•Cr2O3,還含有少量的SiO2、Al2O3),加入純堿、空氣氧化,SiO2,Al2O3分別與Na2CO3反應轉化為可溶性的Na2SiO3和NaAlO2,以及二氧化碳氣體,FeO•Cr2O3,則轉化為Fe2O3、Na2CrO4,加入氫氧化鈉溶液堿浸得渣料Ⅰ為Fe2O3,調節溶液的pH值7~8,使NaAlO2產生氫氧化鋁沉淀,Na2SiO3產生H2SiO3沉淀,所以渣料Ⅱ為Al(OH)3、H2SiO3,在溶液中加入硫酸酸化,得Na2CrO4、Na2SO4混合溶液,根據溶解度曲線圖可知,將溶液蒸發濃縮,趁熱過濾得到晶體a為硫酸鈉晶體,然后將得到的濾液冷卻結晶過濾得到Na2Cr2O7•2H2O,溶液中含有Na2Cr2O7,再回到酸化塔中,進行循環利用,以此解答該題.
解答 解:鉻鐵礦(主要成分:FeO•Cr2O3,還含有少量的SiO2、Al2O3),加入純堿、空氣氧化,SiO2,Al2O3分別與Na2CO3反應轉化為可溶性的Na2SiO3和NaAlO2,以及二氧化碳氣體,FeO•Cr2O3,則轉化為Fe2O3、Na2CrO4,加入氫氧化鈉溶液堿浸得渣料Ⅰ為Fe2O3,調節溶液的pH值7~8,使NaAlO2產生氫氧化鋁沉淀,Na2SiO3產生H2SiO3沉淀,所以渣料Ⅱ為Al(OH)3、H2SiO3,在溶液中加入硫酸酸化,得Na2CrO4、Na2SO4混合溶液,根據溶解度曲線圖可知,將溶液蒸發濃縮,趁熱過濾得到晶體a為硫酸鈉晶體,然后將得到的濾液冷卻結晶過濾得到Na2Cr2O7•2H2O,溶液中含有Na2Cr2O7,再回到酸化塔中,進行循環利用,
(1)試劑X與硫酸均是調節溶液pH的,如果用硫酸直接將溶液pH調整至酸化塔中溶液的pH,則溶液中偏鋁酸鈉會變成鋁離子,無法除去鋁元素,提高鉻元素浸出率的措施是加熱、攪拌、將鉻鐵礦粉碎等,
故答案為:溶液中偏鋁酸鈉會變成鋁離子,無法除去鋁元素;加熱、攪拌、將鉻鐵礦粉碎等;
(2)FeO•Cr2O3與Na2CO3反應被空氣中的氧氣氧化,生成Fe2O3、Na2CrO4,反應的方程式為4FeO•Cr2O3+7O2+8Na2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2Fe2O3+8Na2CrO4+8CO2↑,
故答案為:4FeO•Cr2O3+7O2+8Na2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2Fe2O3+8Na2CrO4+8CO2↑;
(3)酸化時主要反應的離子方程式為2CrO42-+2H+=Cr2O7 2-+H2O,
故答案為:2CrO42-+2H+=Cr2O7 2-+H2O;
(4)根據上面的分析可知,操作Ⅰ的內容是 蒸發濃縮,趁熱過濾,晶體a的化學式是 Na2SO4,進行操作Ⅱ為冷卻結晶過濾,過程中實驗時的溫度最好控制在 50~80℃,溶液b中含有Na2Cr2O7,再回到酸化塔中,使鉻元素充分利用,
故答案為:蒸發濃縮,趁熱過濾;Na2SO4;50~80;使鉻元素充分利用;
(5)鉻鐵礦中鉻元素的質量分數為a%,10t的鉻鐵礦經過上述處理后可得到Na2Cr2O7的質量為0.2at,則轉化過程中鉻元素的利用率為$\frac{\frac{0.2at}{262}×2×52}{10t×a%}$×100%=79.4%,
故答案為:79.4%.
點評 本題考查了物質制備的流程分析判斷,物質性質和實驗操作的分析應用,把握晶體析出的原理和溶解度變化特征的分析是解題關鍵,題目難度中等,側重于考查學生的實驗能力、分析問題、解決問題的能力.


 學期復習一本通學習總動員期末加暑假延邊人民出版社系列答案
學期復習一本通學習總動員期末加暑假延邊人民出版社系列答案 芒果教輔暑假天地重慶出版社系列答案
芒果教輔暑假天地重慶出版社系列答案科目:高中化學 來源: 題型:選擇題
| A. | Na與氧氣反應只生成Na2O2 | |
| B. | 將SO2通入過量CaCl2溶液可生成CaSO3沉淀 | |
| C. | 向Fe(NO3)2溶液滴加稀鹽酸,溶液變黃色 | |
| D. | 向酚酞試液加足量Na2O2粉末,充分振蕩后溶液呈紅色 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 氯元素在自然界中只以化合態形式存在 | |
| B. | H2在Cl2中燃燒會產生蒼白色火焰 | |
| C. | 漂粉精是混合物,其有效成分是次氯酸鈉 | |
| D. | 久置氯水最終變為稀鹽酸 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 增大 | B. | 減小 | C. | 不變 | D. | 前三種均有可能 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 半導體行業中有一句話:“從沙灘到用戶”計算機芯片的材料是二氧化硅 | |
| B. | “人造太陽”原理為:21H+31H→42He+10n,該過程不是化學變化 | |
| C. | “84”消毒液的有效成分是Ca(ClO)2 | |
| D. | “殲-20”飛機上使用的碳纖維是一種新型的有機高分子材料 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 鹽酸滴在大理石上:2H++CO32-═CO2↑+H2O | |
| B. | 硫酸滴在銅片上:Cu+2H+═Cu2++H2↑ | |
| C. | 向NaOH溶液中通入過量CO2:OH-+CO2═HCO3- | |
| D. | 氫氧化鈉與NaHCO3溶液反應:OH-+H+═H2O |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com