
| A. | Na2CO3→NaHCO3 | B. | Fe→FeCl2 | C. | NaCl→Na | D. | Al2O3→Al(OH)3 |
分析 A、碳酸鈉與二氧化碳水溶液反應生成碳酸氫鈉;
B、鐵與三氯化鐵反應生成氯化亞鐵;
C、電解熔融氯化鈉可以生成鈉;
D、Al2O3到Al(OH)3不能一步反應實現.
解答 解:A、碳酸鈉與二氧化碳水溶液反應生成碳酸氫鈉,可以一步實現,符合題意要求,故不選;
B、鐵與三氯化鐵反應生成氯化亞鐵,可以一步實現,符合題意要求,故不選;
C、電解熔融氯化鈉可以生成鈉,能一步反應實現,符合題意,故不選;
D、氧化鋁屬兩性氧化物,能與酸或者堿發生復分解反應生成鹽和水.上述反應中沒有Al(OH)3這種堿的生成,因此由Al2O3到Al(OH)3不能一步反應實現,故選;
故選D.
點評 熟練掌握常見物質的性質與變化規律,是解答此類問題的基本的知識基礎.


 備戰中考寒假系列答案
備戰中考寒假系列答案科目:高中化學 來源: 題型:解答題
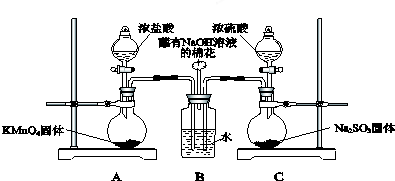
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
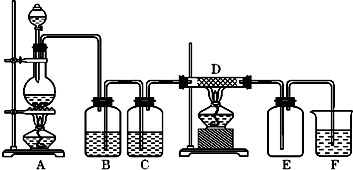
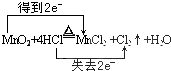 .
.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 電離方程式:Na2SO4═Na2++SO42- | B. | 氯化鈉的電子式: | ||
| C. | 14C的原子結構示意圖: | D. | CH4分子的比例模型: |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| 選項 | 性質 | 原因 |
| A | Fe與稀HNO3、稀H2SO4反應均有氣泡產生 | Fe與兩種酸均發生置換反應 |
| B | 加熱鋁箔,熔化的鋁不滴落 | 鋁表面的氧化膜熔點高,包在熔化的鋁外面 |
| C | 重金屬鹽中毒可服用牛奶解毒 | 牛奶中蛋白質變性,保護了人體的蛋白質 |
| D | 明礬用來凈水 | Al3+水解生成Al(OH)3膠體,具有吸附性 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
| 實驗次數 | 第一次 | 第二次 | 第三次 |
| 消耗高錳酸鉀溶液體積/mL | 25.52 | 25.02 | 24.98 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 醋酸滴在石灰石上:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 鐵與稀鹽酸反應 2Fe+6H+=2Fe3++3H2↑ | |
| C. | 銅片插入硝酸銀溶液中:Cu+2Ag+═2Ag+Cu2+ | |
| D. | 硫酸銅與氫氧化鋇溶液反應:Ba2++SO42-=BaSO4↓ |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com