
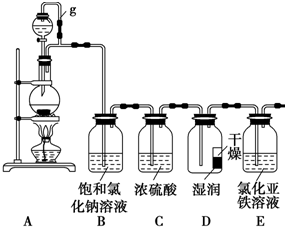
 某探究小組為探究氯氣的性質,設計了如下實驗裝置.請回答下列問題:
某探究小組為探究氯氣的性質,設計了如下實驗裝置.請回答下列問題:分析 (1)①反應中次氯酸鈣中氯元素化合價變化為:+1→0,反應物中氯化氫化合價變化為:-1→0,依據氧化還原反應得失電子守恒,1molCa(ClO)2反應得到2mol電子,則被氧化的氯化氫的物質的量為2mol,生成氯氣物質的量為2mol,依據原子個數守恒配平方程式;
②導氣管將分液漏斗與圓底燒瓶相連,使二者內部壓強相等;
(2)氯氣不能使紅色物質褪色,HClO使有色的物質褪色及水分子的運動來分析;
(3)氯氣具有強的氧化性,能夠氧化氯化亞鐵生成氯化鐵;
(4)氯氣能夠與氫氧化鈉溶液反應生成氯化鈉、次氯酸鈉和水,可以用氫氧化鈉溶液吸收氯氣.
解答 解:(1)①反應中次氯酸鈣中氯元素化合價變化為:+1→0,反應物中氯化氫化合價變化為:-1→0,依據氧化還原反應得失電子守恒,1molCa(ClO)2反應得到2mol電子,則被氧化的氯化氫的物質的量為2mol,生成氯氣物質的量為2mol,依據原子個數守恒反應方程式:Ca(ClO)2+4HCl=2Cl2↑+CaCl2+2H2O;
故答案為:1;4HCl;2;1;2H2O;
②導氣管將分液漏斗與圓底燒瓶相連,使二者內部壓強相等,使濃鹽酸能順利地滴入燒瓶中;
故答案為:平衡壓強,使濃鹽酸能順利地滴入燒瓶中;
(2)實驗進行中氯氣與濕潤紙條中的水生成HClO,使紙條濕潤部分褪色,干燥的部分無水,不能生成HClO所以不褪色,但過一段時間后由于水分子運動,整個紙條都變得濕潤,所以就全部褪色了;
故答案為:不合理; 實驗進行中氯氣與濕潤紙條中的水生成HClO,使紙條濕潤部分褪色,干燥的部分無水,不能生成HClO所以不褪色,但過一段時間后由于水分子運動,整個紙條都變得濕潤,所以就全部褪色了;
(3)氯氣與氯化亞鐵反應生成氯化鐵,化學方程式:2Fe Cl2+Cl2═2FeCl3;
故答案為:2FeCl2+Cl2═2FeCl3;
(4)氯氣能夠與氫氧化鈉溶液反應生成氯化鈉、次氯酸鈉和水,可以用氫氧化鈉溶液吸收氯氣,化學方程式:Cl2+2NaOH=NaCl+NaClO+H2O;
故答案為:Cl2+2NaOH=NaCl+NaClO+H2O.
點評 本題考查氯氣的制取實驗裝置及氯氣的性質,明確裝置的作用及裝置中發生的化學反應即可解答,難度不大.


 新課標同步訓練系列答案
新課標同步訓練系列答案 一線名師口算應用題天天練一本全系列答案
一線名師口算應用題天天練一本全系列答案科目:高中化學 來源: 題型:選擇題
| A. | 氯化銅溶液與鋅粉反應:Cu2++Zn═Zn2++Cu | |
| B. | 稀 H2SO4與鐵粉反應:2Fe2++6H+═Fe3++3H2↑ | |
| C. | 氫氧化鋇溶液與CuSO4 溶液反應:Ba2++SO42-═BaSO4↓ | |
| D. | 碳酸鈣與鹽酸反應:CO32-+2H+═H2O+CO2↑ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.8g | B. | 1.6mg | C. | (2m-3.2g) | D. | (2m-1.6)g |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 實驗室用50mL 0.50 mol•L-1鹽酸、50mL 0.55mol•L-1 NaOH溶液和如圖所示裝置,進行測定中和熱的實驗,得到表中的數據:
實驗室用50mL 0.50 mol•L-1鹽酸、50mL 0.55mol•L-1 NaOH溶液和如圖所示裝置,進行測定中和熱的實驗,得到表中的數據:| 實驗次數 | 起始溫度t1/℃ | 終止溫度t2/℃ | |
| 鹽酸 | NaOH溶液 | ||
| 1 | 20.2 | 20.3 | 23.7 |
| 2 2 | 20.3 | 20.5 | 23.8 |
| 3 | 21.5 | 21.6 | 24.9 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 目前加碘食鹽主要添加的是KIO3 | |
| B. | 鹽鹵可用于制豆腐 | |
| C. | 明礬可用于水的殺菌,消毒 | |
| D. | 在空氣質量日報中SO2含量屬于空氣污染指數 |
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com