
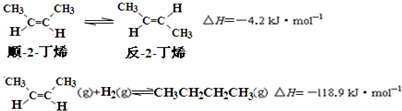
| A. | 反-2-丁烯比順-2-丁烯穩定 | |
| B. | 順-2-丁烯的燃燒熱數值比反-2-丁烯大 | |
| C. | 減壓和升溫有利于平衡向生成正丁烷反應方向移動 | |
| D. | 反-2-丁烯氫化的熱化學方程式為: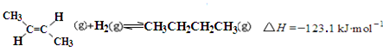 |
分析 A.能量越低越穩定;
B.若生成物相同,反應物的能量高,則放出的熱量多;
C.生成正丁烷的反應為氣體體積減小的放熱反應;
D.蓋斯定律指若一個反應可以分步進行,則各步反應的吸收或放出的熱量總和與這個反應一次發生時吸收或放出的熱量相同.
解答 解:A.順-2-丁烯轉化為反-2-丁烯放熱,說明反-2-丁烯能量低,更穩定,故A正確;
B.等量的順-2-丁烯具有更高的能量.所以順-2-丁烯燃燒熱更大,故B錯誤;
C.生成正丁烷的反應為氣體體積減小的放熱反應,所以減壓向逆向移動,升溫也向逆向移動,所以減壓和升溫不利于平衡向生成正丁烷反應方向移動,故C錯誤;
D.將下式-上式相加得到反-2-丁烯氫化的熱化學方程式,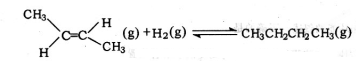 △H=-118.9kJ•mol-1-(-4.2kJ•mol-1)=-114.7kJ•mol-1,故D錯誤.
△H=-118.9kJ•mol-1-(-4.2kJ•mol-1)=-114.7kJ•mol-1,故D錯誤.
故選A.
點評 本題考查能量越低越穩定和蓋斯定律、影響平衡的因素等,難度適中,注意掌握運用蓋斯定律解題.


科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 將水加熱,Kw增大,pH不變 | |
| B. | 向水中加入少量NH4Cl固體,抑制水的電離 | |
| C. | 向水中加入少量NaOH固體,促進水的電離 | |
| D. | 向水中加入少量NaHSO4固體,抑制水的電離,c(H+)增大,Kw不變 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 0.03mol/L | B. | 0.04mol/L | C. | 0.05mol/L | D. | 0.06mol/L |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
 ,下列關于其結構的敘述中,正確的是( )
,下列關于其結構的敘述中,正確的是( )| A. | 甲烷分子是正方形結構 | B. | 甲烷分子是正四面體結構 | ||
| C. | 甲烷分子是極性分子 | D. | 甲烷分子的四個鍵不完全相同 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
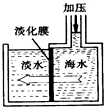 我國有較長的海岸線,浩渺的海洋是一個巨大的物質資源和能量的寶庫.目前,世界各國都在研究如何充分利用海洋資源.
我國有較長的海岸線,浩渺的海洋是一個巨大的物質資源和能量的寶庫.目前,世界各國都在研究如何充分利用海洋資源.查看答案和解析>>
科目:高中化學 來源: 題型:解答題
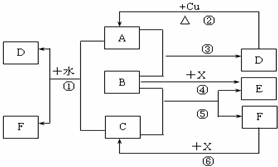
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 若NaHA溶液呈酸性,則H2A一定是強酸 | |
| B. | 若NaHA溶液呈堿性,則H2A一定是弱酸 | |
| C. | NaHA溶液中Na+和HA-的個數之比一定大于1:1 | |
| D. | NaHA晶體中的陰陽離子個數比一定是1:1 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 原子半徑比較:X<Y<Z<W | |
| B. | X2H4與H2W都能使溴水褪色 | |
| C. | X的氫化物的沸點一定低于Y的氫化物的沸點 | |
| D. | 短周期所有元素中,Z的最高價氧化物的水化物堿性最強 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com