

 ,該反應類型為取代反應.
,該反應類型為取代反應. .
. .
. 分析 A的分子式為C4H9Cl,核磁共振氫譜表明其只有一種化學環境的H,則A的結構簡式為:(CH3)3CCl,在氫氧化鈉醇溶液、加熱條件下發生消去反應,生成B,則B為CH2=C(CH3)2,B發生信息中的反應生成的C為(CH3)2CHCH2OH,C發生催化氧化生成D為(CH3)2CHCHO,D再與氫氧化銅反應,酸化得到E為(CH3)2CHCOOH;F的分子式為C7H8O,苯環上的一氯代物只有兩種,應含有2個不同的側鏈,且處于對位,則F為 ,與氯氣在光照條件下發生取代反應,生成G為
,與氯氣在光照條件下發生取代反應,生成G為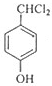 ,G在氫氧化鈉水溶液發生水解反應,酸化得到H,由于同一個碳原子上連有兩個羥基不穩定,易脫水形成羰基,故H為
,G在氫氧化鈉水溶液發生水解反應,酸化得到H,由于同一個碳原子上連有兩個羥基不穩定,易脫水形成羰基,故H為 ,H與E發生酯化反應生成I,其分子中含有醛基和酯基,故I為
,H與E發生酯化反應生成I,其分子中含有醛基和酯基,故I為 ,據此解答.
,據此解答.
解答 解:(1)A的分子式為C4H9Cl,核磁共振氫譜表明其只有一種化學環境的H,則A的結構簡式為:(CH3)3CCl,其名稱為:2-甲基-2-氯丙烷,
故答案為:2-甲基-2-氯丙烷;
(2)A的結構簡式為:(CH3)3CCl,在氫氧化鈉醇溶液、加熱條件下發生消去反應,生成B,則B為CH2=C(CH3)2,B發生信息中的反應生成的C為(CH3)2CHCH2OH,C發生催化氧化生成D,D的結構簡式為:(CH3)2CHCHO,
故答案為:(CH3)2CHCHO;
(3)D再與氫氧化銅反應,酸化得到E為(CH3)2CHCOOH,其分子式為:C4H8O2,
故答案為:C4H8O2;
(4)F生成G的化學方程式為: ,該反應類型為取代反應,
,該反應類型為取代反應,
故答案為: ;取代反應;
;取代反應;
(5)H為 ,H與E發生酯化反應生成I,其分子中含有醛基和酯基,故I為
,H與E發生酯化反應生成I,其分子中含有醛基和酯基,故I為 ,
,
故答案為: .
.
(6)I( )的同系物J比I相對分子質量小14,J比I少一個-CH2-原子團,J的同分異構體中能同時滿足如下條件:①苯環上只有兩個取代基,②既能發生銀鏡反應,又能與飽和NaHCO3溶液反應放出CO2,則J的同分異構體含有-CHO、-COOH,
)的同系物J比I相對分子質量小14,J比I少一個-CH2-原子團,J的同分異構體中能同時滿足如下條件:①苯環上只有兩個取代基,②既能發生銀鏡反應,又能與飽和NaHCO3溶液反應放出CO2,則J的同分異構體含有-CHO、-COOH,
側鏈為-CHO、-CH2CH2COOH,有鄰、間、對三種位置,
側鏈為-CHO、-CH(CH3)COOH,有鄰、間、對三種位置,
側鏈為-CH2CHO、-CH2COOH,有鄰、間、對三種位置,
側鏈為-CH2CH2CHO、-COOH,有鄰、間、對三種位置,
側鏈為-CH(CH3)CHO、-COOH,有鄰、間、對三種位置,
側鏈為-CH3、-CH(CHO)COOH,有鄰、間、對三種位置,
故符合條件的同分異構體有6×3=18種,
J的一個同分異構體發生銀鏡反應并酸化后核磁共振氫譜為三組峰,且峰面積比為2:2:1,而J的同分異構體發生銀鏡反應并酸化后的產物苯環側鏈至少有2種H原子,故產物中苯環上只有1種H原子,產物有2個-COOH,應還含有2個-CH2-,2個側鏈相同且處于對位,產物中側鏈為-CH2COOH,故符合條件的同分異構體結構簡式為: ,
,
故答案為:18; .
.
點評 本題考查有機物推斷,需要對給予的信息進行利用,試題知識點較多、綜合性較強,能較好的考查學生分析、理解能力及邏輯推理能力,題目難度中等,熟練掌握官能團的性質與轉化關系,然后利用正推法推斷即可.


科目:高中化學 來源: 題型:實驗題
 某課外興趣小組欲測定某NaOH溶液的濃度,其操作步驟如下:
某課外興趣小組欲測定某NaOH溶液的濃度,其操作步驟如下:查看答案和解析>>
科目:高中化學 來源: 題型:實驗題

查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 向100mL0.1mol•L-1的Na2CO3溶液中滴加含0.01molCH3COOH的醋酸溶液CO32-+CH3COOH═HCO3-+CH3COO- | |
| B. | 4mol•L-1的NaAlO2溶液和7mol•L-1的鹽酸等體積均勻混合4AlO2-+7H++H2O═3Al(OH)3↓+Al3+ | |
| C. | 等物質的量的FeBr2與Cl2反應:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- | |
| D. | 將少量SO2通入NaClO溶液中:SO2+ClO-+H2O═SO42-+Cl-+2H+ |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 金屬鈉著火,可用泡沫滅火器撲滅 | |
| B. | 用10 mL量筒準確量取7.50 mL稀硫酸 | |
| C. | 用四氯化碳萃取溴水中的溴時,將溴的四氯化碳溶液從分液漏斗下口放出 | |
| D. | 在氫氣還原氧化銅實驗中,先加熱氧化銅,后通入氫氣 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 常溫常壓下,8g甲烷中含C-H鍵的數目為4NA | |
| B. | 25℃時,1L pH=13的Ba(OH)2溶液中含有的OH-數目為0.2NA | |
| C. | 1 mol冰醋酸和1mol乙醇經催化加熱反應生成H2O的分子數為NA | |
| D. | 標準狀況下,2.24L Cl2與過量稀NaOH溶液反應,轉移的電子總數為0.1NA |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 對于相同濃度的弱酸HX和HY(前者的Ka較小)溶液,加水稀釋相同倍數時,HY溶液的pH改變值大于HX溶液的pH改變值 | |
| B. | 在NH3•H2O和NH4Cl濃度均為0.1 mol•L-1的體系中,外加少量酸或堿時,溶液的pH可保持基本不變 | |
| C. | 在NaH2PO4水溶液中存在關系:c(H3PO4)+c(H+)=c(HPO42-)+c(PO43-)+c(OH-) | |
| D. | 沉淀溶解平衡AgI?Ag++I- 的平衡常數為8.5×10-17,不能說明難溶鹽AgI是弱電解質 |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com