
���� ����K2MnO4��Һ��ͨ��CO2���w��ʹ�wϵ�����Ի������ԣ�K2MnO4�l(f��)���绯����������(j��)Ԫ���غ��Լ�������̼�^���Ɯy��������KMnO4��MnO2��KHCO3��
�ڡ�늽ⷨ����F(xi��n)����ˇ����늽�K2MnO4ˮ��Һ����늽����ꖘO��MnO42-ʧȥ��ӣ��l(f��)�������������a(ch��n)��MnO4-����ꎘO��ˮ��x�a(ch��n)����H+�@�����׃?y��u)����ݳ���늘O����ʽ�ǣ�2H2O+2e-=H2��+2OH-��
������(j��)늽ⷨ����ʽ2K2MnO4+2H2O$\frac{\underline{\;ͨ�\;}}{\;}$2KMnO4+2H2��+2KOH����֪K2MnO4����Փ��������100%�����ڶ�����̼�绯��������3K2MnO4+2CO2=2KMnO4+MnO2+K2CO3��K2MnO4����Փ��������$\frac{2}{3}$��
��� �⣺����K2MnO4��Һ��ͨ��CO2���w��ʹ�wϵ�����Ի������ԣ�K2MnO4�l(f��)���绯����������(j��)Ԫ���غ��Լ�������̼�^���Ɯy��������KMnO4��MnO2��KHCO3��
�ʴ𰸞飺KHCO3��
�ڡ�늽ⷨ����F(xi��n)����ˇ����늽�K2MnO4ˮ��Һ����늽����ꖘO��MnO42-ʧȥ��ӣ��l(f��)�������������a(ch��n)��MnO4-��늘O����ʽ�ǣ�MnO42--e-=MnO4-����ꎘO��ˮ��x�a(ch��n)����H+�@�����׃?y��u)����ݳ���늘O����ʽ�ǣ�2H2O+2e-=H2��+2OH-��
�ʴ𰸞飺ꖘO��2H2O+2e-=H2��+2OH-��
������(j��)늽ⷨ����ʽ2K2MnO4+2H2O$\frac{\underline{\;ͨ�\;}}{\;}$2KMnO4+2H2��+2KOH����֪K2MnO4����Փ��������100%�����ڶ�����̼�绯��������3K2MnO4+2CO2=2KMnO4+MnO2+K2CO3��K2MnO4����Փ��������$\frac{2}{3}$�����Զ��ߵ���Փ������֮�Ȟ�3��2��
�ʴ𰸞飺3��2��
�c�u ���}�C�Ͽ������|(zh��)���Ƃ䡢늽��Լ�����߀ԭ����������l���c����(c��)���ڌW���ķ��������Ŀ��飬ע�����Ԫ�ػ��σr��׃���Լ�늽��ԭ�����y�Ȳ���


 ��У��������(y��u)���I(y��)���Ӻ���ԇ��ϵ�д�
��У��������(y��u)���I(y��)���Ӻ���ԇ��ϵ�д� ȫ�̽��ϵ�д�
ȫ�̽��ϵ�д�
| �꼉 | �����n�� | �꼉 | �����n�� |
| ��һ | ��һ���M�n�����]�� | ��һ | ��һ���M�n�����]�� |
| �߶� | �߶����M�n�����]�� | ���� | �������M�n�����]�� |
| ���� | �������M�n�����]�� | ���� | �������M�n�����]�� |
��Ŀ�����л��W ��Դ�� �}�ͣ��x���}
| A�� |  | B�� |  | C�� |  | D�� |  |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ��x���}
| A�� | Ba��OH��2��Һ�cH2SO4��Һ | B�� | Ba��HCO3��2��Һ�cNaOH��Һ | ||
| C�� | �}���cK2CO3��Һ | D�� | FeBr2��Һ�cCl2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ����x�}
| A�� | ���س����£�11.2 Lһ����̼���Ӕ�(sh��)��0.5NA | |
| B�� | NA��������Ӻ�NA��������ӵ��|(zh��)���Ȟ�8��7 | |
| C�� | ���س����£�2.86 g Na2CO3•10H2O���е�Na+��(sh��)��0.02NA | |
| D�� | ���|(zh��)������Ȟ�0.5 mol•L-1��MgCl2��Һ�У�����Cl-����(sh��)��NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ�����}
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ��x���}
| A�� |  �����ӵ��_ | B�� |  �T���з� | C�� |  �w˹ | D�� |  �������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ��x���}
| A�� | ��ˮ�齻�ڣ����ϝ��͡�ǰ�߰�������׃���������߰������W׃�� | |
| B�� | ��������F�����~���l(f��)�����ÓQ���� | |
| C�� | �����Q�����z���M���еġ��z���ĺ͡���ĸ���о������������¡��е��ޡ�������Ҫ�ɷֶ����w�S�� | |
| D�� | ���uˮ�c������һ�オһ���ǰ���Ԓ�c�z�w֪�R���P(gu��n) |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ��x���}
| A�� | CH3COOH--�ƾ� | B�� | CO--ˮú�� | C�� | CaSO3--����ʯ | D�� | Na2CO3--���A |
�鿴�𰸺ͽ���>>
��Ŀ�����л��W ��Դ�� �}�ͣ��Ɣ��}
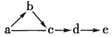 ���У�a�dž��|(zh��)��b�ǚ��w��c��d�������e����߃r���������ˮ���
���У�a�dž��|(zh��)��b�ǚ��w��c��d�������e����߃r���������ˮ����鿴�𰸺ͽ���>>
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��ƽ�_ | �W(w��ng)���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙�(qu��n)�e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com