
短周期主族元素W、R、X、Y、Z,原子序數依次增大。W、X、Y三種元素原子的最外層電子數之和為15,Y原子核電荷數等于W原子核電荷數的2倍,R原子最外層電子數與X原子最外層電子數相差1。下列敘述正確的是
A、R在化合物中顯+1價
B、最高價氧化物的水化物的堿性:X>R
C、原子半徑:X>Y>Z
D、簡單氣態氫化物的沸點:Y>W
科目:高中化學 來源:2015-2016學年內蒙古包頭九中高一下第一次月考化學試卷(解析版) 題型:實驗題
NH3及其鹽都是重要的化工原料。
(1)合成氨工業對化學的國防工業具有重要意義,寫出氨的兩種重要用途 。
(2)用NH4Cl和Ca(OH)2制備NH3,反應發生、氣體收集和尾氣處理裝置依次為 。
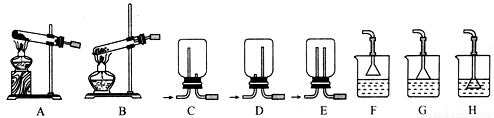
實驗室制備氨氣,下列方法中適宜選用的是 。
①固態氯化銨加熱分解 ②固體氫氧化鈉中滴加濃氨水
③氯化銨溶液與氫氧化鈉溶液共熱 ④加熱農氨水
(3)按下圖裝置進行NH3性質實驗。(已知AB兩瓶容積相同)
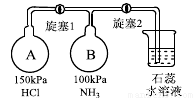
①先打開旋塞1,B瓶中的現象是 ,原因是 ,穩定后,關閉旋塞1。
②再打開旋塞2,B瓶中的現象是 。
(4)某興趣小組在實驗室探究工業合成硝酸的化學原理。
①氨的催化氧化:圖a是探究氨的催化氧化的簡易裝置,實驗中觀察到錐形瓶中鉑絲保持紅熱,有紅棕色氣體生成或白煙產生。白煙的成分是 (填化學式)。
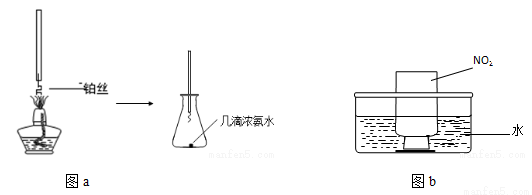
②NO2的吸收:如圖b所示,將一瓶NO2倒置于水槽中,在水下移開玻璃片,可觀察到的現象是 。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年江西省高一下期中化學試卷(解析版) 題型:填空題
某元素M的最高價氧化物為MO2,在其簡單氫化物中M的質量分數為0.75。
(1)M的摩爾質量 。
(2)已知M的原子核內質子數與中子數相等,則元素M的最高價氧化物為 (填“酸性”“堿性”或“兩性”)氧化物,寫出MO2與過量氫氧化鈉溶液反應的離子方程式 。
查看答案和解析>>
科目:高中化學 來源:2015-2016學年江西省高一下期中化學試卷(解析版) 題型:選擇題
下列關于化學用語的表述正確的是
A.HClO的結構式:H-Cl-O
B.純堿的化學式為:Na2CO3
C.原子核內有8個中子的碳原子148C
D.Na2O3電子式為
查看答案和解析>>
科目:高中化學 來源:2015-2016學年江蘇省高一下期中化學試卷(解析版) 題型:選擇題
能夠說明氯的非金屬性比硫強的事實有
①HCl酸性強于H2S的酸性
②將氯氣通入H2S溶液中可置換出硫
③氯氣與鐵反應生成FeCl3,硫與鐵反應生成FeS
④硫和氯變成簡單陰離子時硫原子得到的電子更多
⑤氯氣和氫氣的混合氣,經強光照射可劇烈反應,而硫與氫氣反應需較高溫度
A.②③⑤ B.①③⑤ C.①②③ D.①②③⑤
查看答案和解析>>
科目:高中化學 來源:2015-2016學年江蘇省高一下期中化學試卷(解析版) 題型:選擇題
把A、B、C、D4塊金屬片浸入稀硫酸中,用導線兩輛相連組成原電池。若A、B相連時,A為負極;C、D相連時,D上產生大量氣泡;A、C相連時,電流由C經導線流向A;B、D相連時,H+在溶液中流向B,則此4種金屬的活動性由強到弱的順序為
A.A>B>C>D B.A>C>D>B
C.C>A>B>D D.B>A>C>D
查看答案和解析>>
科目:高中化學 來源:2015-2016學年江蘇省高一下期中化學試卷(解析版) 題型:選擇題
元素周期表是學習化學的重要工具,下圖是元素周期表中的一格,以下對該圖信息的解讀中,不正確的是
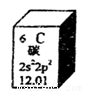
A.該元素的原子序數為6
B.該元素所有原子的質子數均為6
C.該元素的原子質量為12.01 g
D.該元素應有多種同位素,所有原子的中子數不都為6
查看答案和解析>>
科目:高中化學 來源:2015-2016學年黑龍江雙鴨山一中高二下期中化學試卷(解析版) 題型:選擇題
某有機物的結構簡式為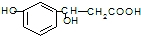 ,它可以發生反應的類型有( )
,它可以發生反應的類型有( )
①加成 ②消去 ③水解 ④酯化 ⑤氧化 ⑥加聚.
A.①②⑤⑥ B.③④⑤⑥ C.①②③④ D.①②④⑤
查看答案和解析>>
科目:高中化學 來源:2016屆海南省高三高考考前模擬十二化學試卷(解析版) 題型:填空題
X、Y、Z、R、M是原子序數依次增大五種元素,基態X原子的s電子數比p電子數多3個,在周期表中Y與Z相鄰且第一電離能Y>Z,Z、R同主族,M核外電子有29種運動狀態,請回答下列問題:
(1)基態M2+的電子排布式為__________,X、Y、Z、M的電負性由大到小的順序為__________。
(2)化合物XCl3的中心原子雜化類型為__________;YCl3的立體構型為__________,XCl3、YCl3分子中屬于非極性分子的是__________。
(3)H2Z、H2Z2、H2R的沸點分別為100℃、158℃,-60.4℃,試解釋此種現象____________。
(4)H2RO3的K1和K2分別為1.54×10-2和1.02×10-7,熔融化狀態下RO3不能導電而Na2O能導電,請根據結構與性質的關系解釋下列問題:
①K1>K2:____________。
②RO3不能導電而Na2O能導電:____________。
(5)Z、M形成的一種化合物晶胞如圖所示: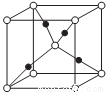 (實心球代表M)
(實心球代表M)
①該化合物的化學式為_______________。
②若晶胞參數為apm。列式計算該晶胞的密度籽=____g·cm-3。
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com