
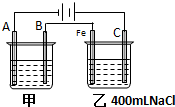
 如圖為相互串聯的甲、乙兩電解池試回答:
如圖為相互串聯的甲、乙兩電解池試回答:分析 根據電源的正負極可判斷A、B、Fe、C分別為電解池的陰極、陽極、陰極、陽極,在陰極上發生還原反應,在陽極上發生氧化反應,乙池反應中陰極:2H2O+2e-═H2↑+20H-,陽極:2Cl--2e-═Cl2↑,若甲為用電解原理給鐵片鍍銀的裝置,陰極反應為Ag++e-=Ag,陽極反應為Ag-e-=Ag+,電解質溶液應選與鍍層具有相同金屬離子的可溶性鹽溶液;然后根據電極反應以及兩個串聯電解池轉移電子數目相等計算.
解答 解:(1)根據電源的正負極可判斷A、B、Fe、C分別為電解池的陰極、陽極、陰極、陽極,在陰極上發生還原反應,在陽極上發生氧化反應,在鐵片上鍍銀時,鍍層金屬銀為電解池的陽極,陽極上的電極反應式為Ag-e-=Ag+,鍍件金屬鐵為電解池的陰極,陰極上的電極反應式Ag++e-=Ag,電解質溶液含有鍍層金屬離子,應為可溶性硝酸銀溶液.
故答案為:鐵;Ag++e-=Ag;Ag;Ag-e-=Ag+;AgNO3溶液;
(2)乙池電解NaCl溶液,陰極鐵電極反應為:2H2O+2e-═H2↑+20H-,滴加酚酞溶液后,陰極溶液變紅.故答案為:Fe;
(3)甲槽陰極反應為Ag++e-=Ag,陰極增重43.2g,應為銀的質量,n=$\frac{43.2g}{108g/mol}$=0.4 mol,轉移的電子為0.4mol,兩個電解池串聯,轉移的電子數目相等,乙槽陽極反應為2Cl--2e-═Cl2↑,轉移的電子為0.4mol時,在陽極上生成氣體的物質的量為0.2mol,
放出氣體在標準狀況下的體積為0.2mol×22.4L/mol=4.48L.
故答案為:4.48.
點評 本題考查了電鍍原理及氧化還原反應的有關計算,難度不大,注意串聯電解池得失電子數相等的特點.


科目:高中化學 來源: 題型:選擇題
| A. | 電解飽和食鹽水可冶煉金屬鈉 | |
| B. | 氧化鈉可用于呼吸面具 | |
| C. | 鋁熱反應中的鋁熱劑是混合物 | |
| D. | 凡含有添加劑的食物對人體健康均有害,不宜食用 |
查看答案和解析>>
科目:高中化學 來源: 題型:選擇題
| A. | 摩爾既是物質的數量單位又是物質的質量單位 | |
| B. | 常溫常壓下,48gO2所占的體積是33.6L | |
| C. | 阿伏加德羅常數的數值就是0.012kg12C中含有的碳原子數目 | |
| D. | 把1molNaCl溶于1L水中,所得溶液物質的量濃度為1mol/L |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
 一份溶液中可能含有K+、Al3+、H+、NH4+、Cl-、Br-、I-、ClO-、AlO2- 等離子中的若干種.為了確定溶液的組成,進行了如下操作:
一份溶液中可能含有K+、Al3+、H+、NH4+、Cl-、Br-、I-、ClO-、AlO2- 等離子中的若干種.為了確定溶液的組成,進行了如下操作:| Cl2的體積(標況下) | 2.8L | 5.6L | 11.2L |
| n(Cl- ) | 1.25mol | 1.5mol | 2mol |
| n(Br- ) | 1.5mol | 1.4mol | 0.9mol |
| n(I- ) | a mol | 0 | 0 |
查看答案和解析>>
科目:高中化學 來源: 題型:多選題
| A. | 98.3%的硫酸加入到稀氫氧化鋇溶液中:H+(aq)+OH-(aq)═H2O(l)△H=-57.3kJ/mol | |
| B. | 向NH4Fe(SO4)2溶液中逐滴加入Ba(OH)2溶液,可能發生的反應是:3NH4++Fe3++3SO42-+3Ba2++6OH-═3BaSO4↓+Fe(OH)3↓+3NH3•H2O | |
| C. | 酸化的淀粉碘化鉀溶液在空氣中變藍:4I-+O2+4H+═2I2+2H2O | |
| D. | Na2SO3溶液使酸性KMnO4溶液褪色:5SO32-+6H++2MnO4-═5SO42-+2Mn2++3H2O |
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:解答題
查看答案和解析>>
科目:高中化學 來源: 題型:填空題
 實驗室制備1,2-二溴乙烷的反應原理如下:
實驗室制備1,2-二溴乙烷的反應原理如下:| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 狀態 | 無色液體 | 無色液體 | 無色液體 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸點/℃ | 78.5 | 132 | 34.6 |
| 熔點/℃ | -130 | 9 | -116 |
查看答案和解析>>
湖北省互聯網違法和不良信息舉報平臺 | 網上有害信息舉報專區 | 電信詐騙舉報專區 | 涉歷史虛無主義有害信息舉報專區 | 涉企侵權舉報專區
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com